Глава 9. Аортальный клапан и корень аорты
Глава 9. Аортальный клапан и корень аорты
Исследование аортального клапана стало сильной стороной эхокардиографии со времени ее внедрения в клиническую практику в начале 70-х годов. Поначалу была показана надежность М-модальной эхокардиографии для исключения аортального стеноза и высокая чувствительность ее в диагностике аортальной недостаточности. С появлением двумерного, а затем и различных допплеровских режимов, оказалось, что эхокардиография настолько хорошо диагностирует патологию аортального клапана, что превосходит по своей диагностической ценности катетеризацию сердца и ангиографию.
Нормальный аортальный клапан и корень аорты
Исследование аортального клапана начинается с визуализации его из парастернального доступа в позиции длинной оси левого желудочка. Затем под контролем двумерного изображения, обычно по парастернальной короткой оси на уровне основания сердца, луч М-модального исследования направляется на створки аортального клапана и корень аорты (рис. 2.2). На рис. 2.6 представлен аортальный клапан из позиции парастернальной короткой оси и М-модальное его изображение. В срез М-модального изображения попадают правая коронарная и некоронарная створки аортального клапана. Линия их смыкания в диастолу в норме находится посередине между передней и задней стенками аорты. В систолу створки открываются и, расходясь кпереди и кзади, образуют «коробочку». В таком положении створки остаются до конца систолы. В норме при М-модальном исследовании может регистрироваться легкое систолическое дрожание створок аортального клапана.
Если неизмененные тонкие створки аортального клапана открываются не полностью, это обычно означает резкое снижение ударного объема. При нормальном ударном объеме и дилатации корня аорты створки клапана, раскрываясь, могут несколько отстоять от стенок аорты. При низком ударном объеме М-модальное движение створок аортального клапана иногда имеет форму треугольника: сразу после полного раскрытия створки начинают закрываться. Если створки резко захлопываются после максимального их раскрытия, следует заподозрить фиксированный подклапанный стеноз. Средне-систолическое прикрытие створок аортального клапана (частичное закрытие их в середине систолы, затем — вновь максимальное раскрытие) является признаком динамического подклапанного стеноза, т. е. гипертрофической кардиомиопатии с обструкцией выносящего тракта левого желудочка. В диастолу закрытые створки параллельны стенкам аорты. Диастолическое дрожание створок аортального клапана свидетельствует о серьезной патологии и наблюдается при разрыве или отрыве створок. Эксцентрическое расположение линии смыкания створок аортального клапана заставляет заподозрить врожденную патологию — двустворчатый аортальный клапан.
Движение корня аорты может дать ценную информацию о глобальной систолической и диастолической функции левого желудочка. В норме корень аорты смещается кпереди в систолу более, чем на 7 мм, и почти немедленно возвращается на место по ее окончании. Движения корня аорты отражают процессы наполнения и опорожнения левого предсердия; во время предсердной систолы в норме они минимальны. При уменьшении амплитуды движения корня аорты следует думать о низком ударном объеме. Заметим, что амплитуда движения корня аорты не имеет прямой зависимости от фракции выброса. Например, при гиповолемии и нормальной сократимости левого желудочка амплитуда движения корня аорты уменьшается. Нормальная или даже чрезмерная подвижность корня аорты при уменьшенном раскрытии створок аортального клапана свидетельствует о диспропорции между кровотоком в левом предсердии и в аорте и наблюдается при тяжелой митральной недостаточности.
При двумерном исследовании парастернально по короткой оси аортальный клапан выглядит как структура, состоящая из трех симметрично расположенных, одинаково тонких створок, в систолу они полностью открывающихся, а в диастолу закрываются и образуют фигуру, похожую на перевернутую эмблему автомобиля Mercedes-Benz. Место смыкания всех трех створок может выглядеть чуть утолщенным. Корень аорты имеет диаметр больший, чем остальная часть восходящего отдела аорты, и формируется из трех синусов Вальсальвы, которые называются аналогично створкам клапана: левый коронарный, правый коронарный, некоронарный. В норме диаметр корня аорты не превышает 3,5 см. Допплеровское исследование кровотока через аортальный клапан дает спектр треугольной формы; максимальная скорость аортального кровотока — от 1,0 до 1,5 м/с. Аортальный клапан имеет меньший диаметр, чем выносящий тракт левого желудочка и восходящий отдел аорты, поэтому скорость кровотока выше всего именно на уровне клапана.
Аортальный стеноз
Эхокардиография, включающая допплеровское исследование в постоянно-волновом режиме, — очень надежный метод диагностики и оценки тяжести аортального стеноза. Метод позволяет измерить систолический градиент между левым желудочком и аортой и вычислить площадь отверстия аортального клапана.
М-модальное исследование при аортальном стенозе выявляет изменения структуры и движения створок клапана: регистрируются плотные, неоднородные сигналы, уменьшается систолическое раскрытие створок. Однако уплотнение и утолщение стенок аорты и створок аортального клапана может дать сходную картину и в отсутствии гемодинамически значимого стеноза. Поэтому нельзя ориентироваться только на М-модальные измерения раскрытия створок аортального клапана. Тем не менее при невозможности проведения допплеровского исследования иногда приходится высказывать суждение о тяжести стеноза по раскрытию створок аортального клапана. При этом исходят из того, что раскрытие створок, превышающее 12 мм, почти всегда свидетельствует об отсутствии значимого стеноза, раскрытие менее 8 мм, наоборот, почти всегда свидетельствует о тяжелом аортальном стенозе; промежуточные значения (от 8 до 12 мм) могут соответствовать стенозу любой степени выраженности.
Двумерное исследование больного с предполагаемым аортальным стенозом имеет целью определение степени кальциноза корня аорты и, что еще важнее, формы и движения створок аортального клапана. Если видна четкая граница между створками и каждая из них движется в своем направлении, то тяжелый аортальный стеноз исключен. Если же, напротив, наблюдается куполообразное закругление створок и они движутся в одном направлении, то вероятность тяжелого аортального стеноза существенно возрастает.
О гемодинамической значимости аортального стеноза можно судить по таким показателям как наличие или отсутствие постстенотического расширения аорты, толщина стенок и масса миокарда левого желудочка, размер левого предсердия. Постстенотическое расширение аорты почти всегда присутствует при тяжелом аортальном стенозе. У клинически компенсированных пациентов с гемодинамически значимым аортальным стенозом обычно выявляется гипертрофия левого желудочка и повышение его глобальной сократимости. Повышенная сократимость кажется парадоксальным явлением в условиях хронического повышения посленагрузки. Возможное объяснение повышенной сократимости левого желудочка при аортальном стенозе состоит в том, что напряжение стенки левого желудочка [wall stress] у этих пациентов в покое снижено; повышенную сократимость можно рассматривать как компенсаторный механизм, обеспечивающий адекватный сердечный выброс при физической нагрузке. Если при тяжелом аортальном стенозе гипертрофия левого желудочка незначительна или отсутствует, то можно ожидать тяжелых клинических проявлений порока.
Количественная оценка тяжести аортального стеноза с помощью допплер-эхокардиографии — одна из самых эффективных областей применения метода. При постоянно-волновом исследовании для измерения градиентов давления между левым желудочком и аортой и расчета площади аортального отверстия необходимо направить ультразвуковой луч точно по потоку стенотической струи. Поэтому у каждого пациента следует искать стенотическую струю из нескольких доступов [134]: апикального, супрастернального и правого парастернального (рис. 9.1, 9.2). Наибольшую скорость кровотока через стенозированный аортальный клапан обычно удается зарегистрировать при исследовании из апикального доступа. В каждом случае мы рекомендуем использовать датчик, предназначенный исключительно для постоянно-волнового исследования: благодаря небольшой поверхности этого датчика, его луч легко направить параллельно стенотической струе, особенно при супрастернальном исследовании. Неточная ориентация ультразвукового луча (под углом к стенотической струе) приводит к недооценке тяжести аортального стеноза.
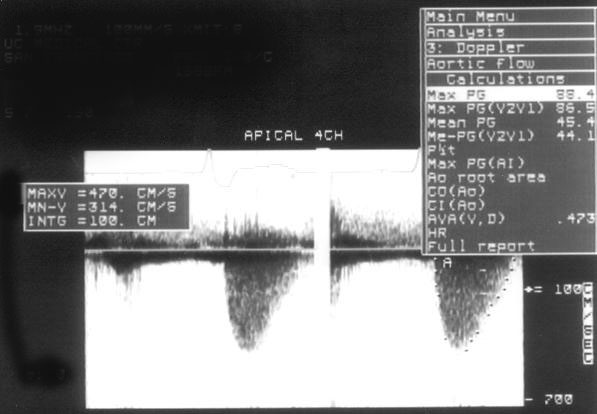
Рисунок 9.1. Аортальный стеноз: постоянно-волновое допплеровское исследование, апикальный доступ. Максимальная скорость аортального кровотока — 4,7 м/с (максимальный градиент между левым желудочком и аортой — 88 мм рт. ст.).
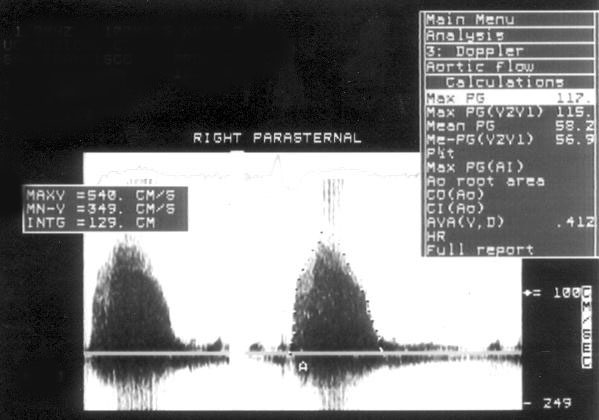
Рисунок 9.2. Аортальный стеноз: постоянно-волновое допплеровское исследование того же пациента, что и на рис. 9.1, правый парастернальный доступ. Как правило, исследование из апикального доступа позволяет получить наиболее высокие (самые близкие к истинным) скорости аортального кровотока; данный пример, однако, свидетельствует о том, что это не всегда верно: при исследовании из правого парастернального доступа зарегистрирована максимальная скорость аортального кровотока равная 5,4 м/с (максимальный градиент давления — 117 мм рт. ст.). В случаях аортального стеноза нужно проводить исследование аортального кровотока из всех возможных позиций (апикальной, правой парастернальной и супрастернальной).
На рис. 9.3 представлен допплеровский аортальный кровоток при аортальном стенозе и расчет максимального градиента давления между левым желудочком и аортой. Заметим, что тот градиент давления, который определяется при катетеризации сердца, не полностью соответствует градиенту, вычисляемому при допплеровском исследовании. При катетеризации вычисляют разность между максимумами давления в левом желудочке и в аорте. Кривые давления в желудочке и аорте, однако, достигают своего пика не одновременно. Допплеровские же вычисления основаны на определении максимальной скорости кровотока через аортальный клапан, а следовательно, — максимальной разности давлений между левым желудочком и аортой [101].
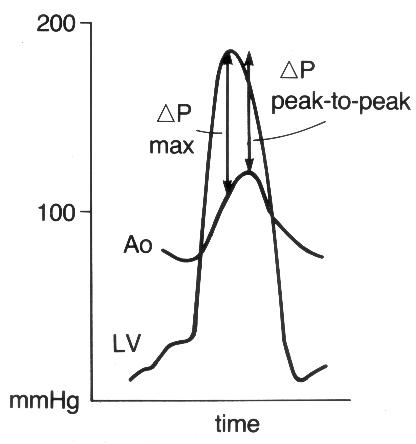
Рисунок 9.3. Аортальный стеноз. Кривые давления в аорте и в левом желудочке достигают максимума не одновременно: в аорте позже, чем в левом желудочке. При катетеризации сердца измеряют значения максимального давления в аорте, затем в левом желудочке и вычисляют их разность. При допплеровском исследовании измеряют максимальную скорость в аорте, которая соответствует максимальному градиенту давления между левым желудочком и аортой. Поэтому при аортальном стенозе допплеровское исследование должно давать более высокие значения максимального градиента давления между левым желудочком и аортой, чем катетеризация сердца. Ao — кривая давления в аорте, LV — кривая давления в левом желудочке, Pmax — максимальный градиент давления (измеряется при допплеровском исследовании), Ppeak-to-peak — разница максимальных давлений (измеряется при катетеризации сердца). Judge K.W., Otto C.M. Doppler echocardiographic evaluation of aortic stenosis, in: Doppler Echocardiography, ed. Schiller N.B., Cardiology Clinics, 8(2), 1990.
В целом, скорость кровотока через аортальный клапан, превышающая 4 м/с, указывает на критический, требующий протезирования клапана, аортальный стеноз; скорости ниже 3 м/с — на нетяжелый стеноз. Для суждения о тяжести порока при промежуточных значениях скорости стенотической струи (от 3 до 4 м/с) требуются дополнительные данные: площадь аортального отверстия, параметры глобальной сократимости левого желудочка и степень аортальной регургитации.
Учитывая, что максимальный градиент давления между левым желудочком и аортой зависит от преднагрузки, посленагрузки и глобальной сократимости левого желудочка, при пограничных значениях градиента бывает трудно отличить умеренно выраженный аортальный стеноз от критического. Существует три возможных решения этой проблемы.
1. Изучение формы допплеровского спектра стенотической струи. Быстрое достижение пика скорости стенотической струи указывает на стеноз скорее умеренный, чем критический. Та же максимальная скорость при медленном ее нарастании может означать критический аортальный стеноз.
2. Определение среднего систолического градиента давления между левым желудочком и аортой. В современных эхокардиографах предусмотрена возможность определения среднего градиента, который вычисляется из интеграла линейной скорости стенотической струи, зарегистрированной в постоянно-волновом режиме. Значения среднего систолического градиента точнее соответствуют данным катетеризации сердца, чем значения максимального градиента.
3. Лучший показатель степени тяжести аортального стеноза — это площадь аортального отверстия [112, 126]. Наиболее распространены способы вычисления площади аортального отверстия из уравнения непрерывности кровотока либо модифицированного уравнения Горлина (рис. 9.4). В табл. 13 приведен перечень измерений, которые необходимо произвести при допплеровском исследовании пациента с аортальным стенозом.
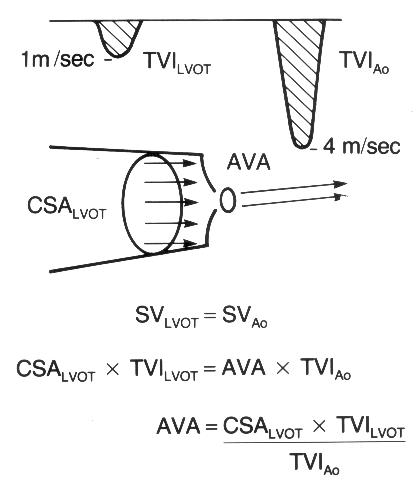
Рисунок 9.4. Допплеровский расчет площади отверстия аортального клапана. Измерения основаны на том, что объем кровотока (ударный объем) в аорте и в выносящем тракте левого желудочка равны между собой. SVLVOT — ударный объем кровотока в выносящем тракте левого желудочка, SVAo — ударный объем кровотока в аорте, AVA — площадь отверстия аортального клапана, CSALVOT — площадь поперечного сечения выносящего тракта левого желудочка, TVIAo — интеграл линейной скорости аортального кровотока, TVILVOT — интеграл линейной скорости кровотока в выносящем тракте левого желудочка. Judge K.W., Otto C.M. Doppler echocardiographic evaluation of aortic stenosis, in: Doppler Echocardiography, ed. Schiller N.B., Cardiology Clinics, 8(2), 1990.
Таблица 13. Параметры, определяемые при допплеровском исследовании пациента с аортальным стенозом
Позиции и измерения 1. Максимальная скорость и наилучшего качества спектр кровотока дистальнее аортального клапана в постоянно-волновом режиме в любой из позиций: апикальной, правой парастернальной, супрастернальной 2. Максимальная скорость и наилучшего качества спектр кровотока в выносящем тракте ЛЖ из апикального доступа в импульсном режиме 3. Диаметр поперечного сечения выносящего тракта ЛЖ, измеряемый в позиции длинной оси ЛЖ парастернально в двумерном режиме Расчетные параметры 1. Максимальный и средний градиент давления между ЛЖ и аортой 2. Площадь отверстия аортального клапана с помощью модифицированного уравнения Горлина либо закона непрерывности потока: Уравнение непрерывности потока: AVA = (CSALVOT?TVILVOT)/TVIAo Модифицированное уравнение Горлина: AVA = (VmeanLVOT?CSALVOT)/VmeanAo ЛЖ — левый желудочек AVA — площадь отверстия аортального клапана CSALVOT — площадь поперечного сечения выносящего тракта ЛЖ TVIAo — интеграл линейной скорости аортального кровотока TVILVOT — интеграл линейной скорости кровотока в выносящем тракте ЛЖ VmeanAo — средняя скорость аортального кровотока VmeanLVOT — средняя скорость в выносящем тракте левого желудочка в систолуНа точность вычисления площади отверстия аортального клапана не влияет наличие или отсутствие у пациента аортальной недостаточности. Неопределенность в вычисление площади аортального отверстия может внести мерцательная аритмия. Следует помнить о возможном сочетании субаортального стеноза с клапанным пороком: градиент давления по разные стороны аортального клапана в этом случае вычисляют не по укороченному, а по полному варианту модифицированного уравнения Бернулли (гл. 3).
Для решения вопроса о необходимости протезирования аортального клапана по поводу аортального стеноза у взрослого пациента мы рекомендуем пользоваться приведенной ниже схемой 9.1.
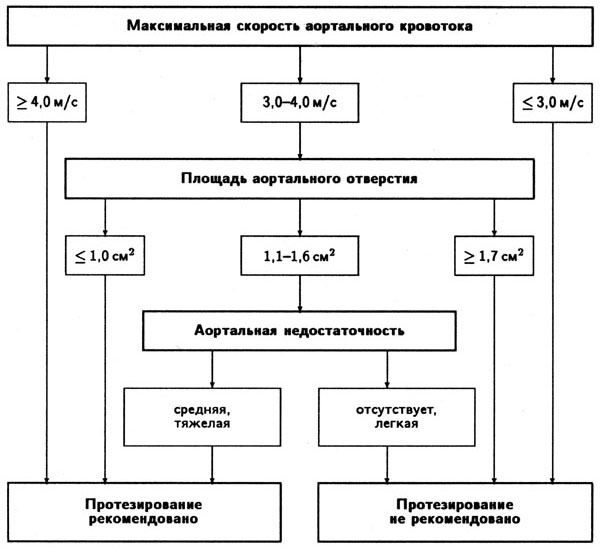
Схема 9-1. Схема решения вопроса о необходимости протезирования аортального клапана по поводу аортального стеноза. Judge KW, Otto CM. Doppler echocardiographic evaluation of aortic stenosis, in Doppler Echocardiography, ed. Schiller NB, Cardiology Clinics, 8(2), 1990.
Определение этиологии аортального стеноза
У большей части больных преклонного возраста с аортальным стенозом при эхокардиографии обнаруживается выраженный кальциноз корня аорты и створок аортального клапана. Эти дегенеративные процессы неспецифичны и потому не могут служить признаком, позволяющим установить причину поражения аортального клапана.
Двустворчатый аортальный клапан — самый распространенный из врожденных пороков сердца (его имеют около 2% людей) и, вероятно, главный предвестник аортального стеноза. При М-модальном исследовании этот порок выявляется по эксцентрическому расположению линии смыкания створок аортального клапана. С еще большей уверенностью его можно диагностировать при двумерном исследовании по невозможности визуализации более чем двух створок и одной комиссуры (рис. 9.5). По нашему мнению, если единственная комиссура двустворчатого аортального клапана расположена вертикально, вероятность ошибочного диагноза меньше, чем при ее горизонтальном расположении. Визуализация трех комиссур еще не является гарантией того, что аортальный клапан трехстворчатый. Одна из комиссур может быть заросшей, и клапан, на самом деле двустворчатый, будет казаться нормальным. Два признака позволяют в этих случаях распознать двустворчатый аортальный клапан: очевидная разница в размерах створок и эксцентрическое их раскрытие. В анамнезе пациентов с аортальным стенозом двустворчатого клапана часто имеются указания на выслушивавшийся в течение многих лет шум в сердце. Трудно сказать, насколько часто аортальный стеноз имеет такую этиологию: если шум появился поздно и пациент страдал артериальной гипертонией, то в основе аортального стеноза могут лежать первичные дегенеративные изменения ранее нормального клапана.
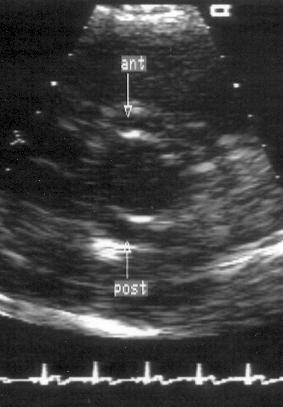
Рисунок 9.5. Некальцифицированный двустворчатый аортальный клапан: парастернальная позиция по короткой оси аортального клапана. Видны только две створки клапана: передняя и задняя. ant — передняя створка, post — задняя створка.
Ревматический аортальный стеноз похож на описанные выше анатомические формы порока, но ревматическое поражение клапана, во-первых, реже приводит к критическому стенозу, во-вторых, часто сопровождается митральным пороком сердца. При ревматической этиологии аортального стеноза больше выражена тенденция к поражению створок, чем аортального кольца, тогда как для дегенеративных процессов характерно преимущественное поражение аортального кольца с последующим распространением процесса на створки — от периферии к центру.
Фиксированный субаортальный стеноз — это сравнительно редкая врожденная патология, имеющая две анатомические разновидности. Самый частый вариант фиксированного субаортального стеноза — подклапанная мембрана [175]; при двумерном исследовании она видна сразу под аортальным клапаном (рис. 9.6). Другой вариант субаортального стеноза — длинный узкий фибромышечный канал, диаметр которого остается неизменным во время всего сердечного цикла. Степень сужения выносящего тракта трудно определить при двумерном исследовании. Допплеровское исследование стеноза проводится по той же методике, что и при клапанном стенозе.
Эхокардиографическая диагностика динамического подклапанного стеноза (обструктивной гипертрофической кардиомиопатии) обсуждается в гл. 5.
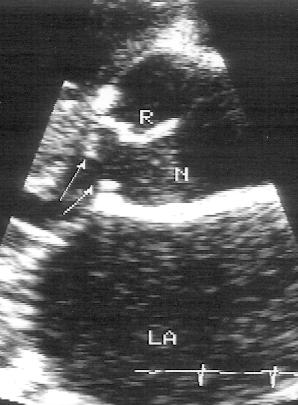
Рисунок 9.6. Врожденный субаортальный («фиксированный») стеноз: подклапанная мембрана (стрелки). Фрагмент изображения, полученного при двумерном исследовании в позиции парастернальной длинной оси левого желудочка. LA — левое предсердие, R — правая коронарная створка аортального клапана, N — некоронарная створка аортального клапана. Материал предоставил проф. Norman H. Silverman.
Аортальная недостаточность
Аортальная регургитация является частой эхокардиографической находкой и почти всегда указывает на патологию. В большинстве случаев эхокардиография позволяет выявить изменения аортального клапана или восходящего отдела аорты, ставшие причиной аортальной регургитации, и установить степень ее выраженности.
При М-модальном исследовании главным признаком аортальной регургитации служит диастолическое дрожание передней створки аортального клапана. Надежность этого симптома в течение долгого времени оставалась неясной. В настоящее время установлено, что наличие или отсутствие диастолического дрожания передней створки митрального клапана при аортальной регургитации зависит от того, какая створка клапана поражена, и это же определяет направление регургитирующей струи. Цветное допплеровское сканирование выявляет большое разнообразие направления регургитирующей струи у разных пациентов (рис. 9.7, 17.16, 17.17); когда она направлена в сторону передней створки митрального клапана, то наблюдается дрожание створки. С появлением двумерной эхокардиографии М-модальные исследования начали регистрировать не на дорогостоящей фотобумаге, а на видеопленке. Это привело к тому, что диастолическое дрожание передней створки митрального клапана стали выявлять реже, из-за относительно низкой временной разрешающей способности видеозаписи. При тяжелой аортальной недостаточности М-модальное исследование регистрирует также раннее закрытие митрального клапана [84]; эта находка свидетельствует о нарушениях гемодинамики, требующих активного медикаментозного и хирургического лечения.
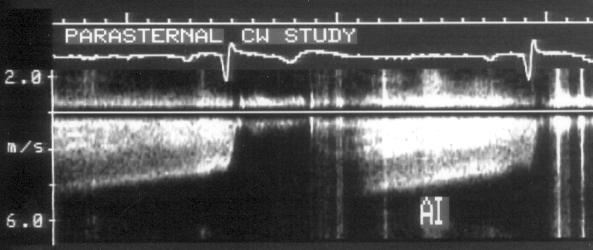
Рисунок 9.7. Эксцентрически направленная аортальная регургитация: постоянно-волновое допплеровское исследование из парастернального доступа. Иногда (например, при пролабировании одной из створок аортального клапана) струя аортальной регургитации направлена эксцентрически. В таких случаях цветное сканирование позволяет правильно ориентировать ультразвуковой луч при постоянно-волновом исследовании. В данном случае струя аортальной регургитации направлена в сторону передней створки митрального клапана. AI — струя аортальной регургитации.
Появление эхокардиографии возбудило интерес к мониторированию размеров левого желудочка у больных с аортальной недостаточностью с целью определения оптимального момента для хирургического лечения [132]. Долгое время считалось, что конечно-систолический размер левого желудочка равный 55 мм указывает на необходимость операции, так как за этим пределом прогноз как естественного течения заболевания, так и результатов операции резко ухудшается. В настоящее время, однако, критическая граница указывающая на необходимость проведения оперативного лечения, отодвинулась; с разработкой новых методов интраоперационной защиты миокарда конечно-систолический размер левого желудочка, равный 55 мм, уже не представляется критическим [91, 99, 138].
Параметры, характеризующие тяжесть аортальной недостаточности, применительно к двумерной эхокардиографии разработаны не так хорошо, как для М-модального исследования. Естественно предположить, что изучение сократимости левого желудочка, его объема, формы и массы (гл. 5) может дать ценную информацию для определения тяжести аортальной недостаточности. С помощью двумерной эхокардиографии можно было бы изучать выраженность объемной перегрузки левого желудочка, отношение его объема к массе, но таких исследований проведено мало. С появлением допплеровских методов двумерная эхокардиография при аортальной недостаточности применяется в основном для выяснения ее генеза.
Допплеровскому исследованию принадлежит главная роль в диагностике аортальной недостаточности и определении ее тяжести. Импульсное допплеровское исследование и особенно цветное сканирование оказались чувствительнее всех существующих методов диагностики аортальной недостаточности, включая инвазивные методы. При выполнении импульсного допплеровского исследования контрольный объем помещают в выносящий тракт левого желудочка под местом смыкания створок аортального клапана (рис. 9.8). Этот прием повторяют из нескольких эхокардиографических позиций, чтобы быть уверенным в том, что учтены все возможные направления регургитирующей струи. Чаще всего лучшей оказывается апикальная пятикамерная позиция сердца. При обнаружении регургитации, занимающей всю диастолу на допплеровском спектре, контрольный объем перемещают по желудочку, чтобы установить глубину проникновения в него регургитирующей струи. Если струя заходит более чем на одну треть глубины желудочка, степень аортальной недостаточности редко бывает легкой. Цветное сканирование, впрочем, полностью заменяет исследования регургитации в импульсном допплеровском режиме. Цветное сканирование быстро и надежно выявляет любую регургитацию, от незначительной до тяжелой, и, кроме того, позволяет точно направить ультразвуковой луч при постоянно-волновом допплеровском исследовании [90, 117] (рис. 17.16, 17.17).
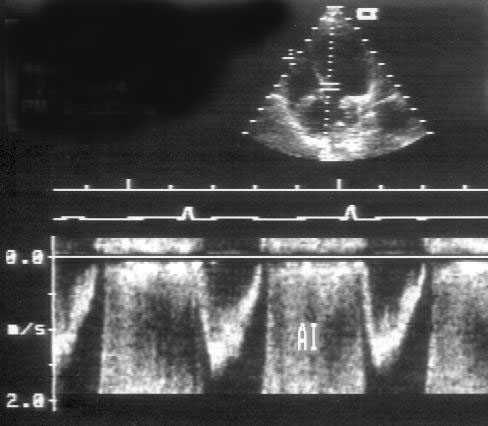
Рисунок 9.8. Аортальная регургитация: импульсное допплеровское исследование. Контрольный объем помещен в выносящий тракт левого желудочка у места смыкания створок аортального клапана. Струя аортальной регургитации появляется сразу после закрытия аортального клапана и в импульсном режиме дает искажение допплеровского спектра. AI — струя аортальной регургитации.
Аортальная регургитация при цветном сканировании выглядит как пестрый патологический диастолический поток, исходящий из аортального клапана и проникающий в левый желудочек. Этот поток отличается от регистрируемого при митральном стенозе тем, что он исходит от аортального клапана и появляется в самом начале диастолы, в фазу изоволюметрического расслабления, когда митральный клапан еще закрыт. В отличие от митральной регургитации, при аортальной максимальная глубина проникновения струи в левый желудочек и площадь, которую струя занимает, не всегда хорошо коррелируют с ангиографической оценкой степени аортальной недостаточности. Более достоверные признаки степени аортальной недостаточности — ширина струи в месте ее формирования и площадь, занимаемая ею при исследовании в позиции парастернальной короткой оси на уровне аортального клапана.
Существует несколько конкурирующих по своей надежности способов оценить тяжесть аортальной недостаточности. Самыми распространенными и, с нашей точки зрения, лучшими являются следующие два способа: 1) измерение времени полуспада (T1/2) диастолического градиента давления между аортой и левым желудочком по исследованию допплеровского спектра аортальной регургитации, зарегистрированного в постоянно-волновом режиме; 2) поиск ретроградного кровотока в нисходящем отделе аорты (из супрастернального доступа). В табл. 14 приведен перечень измерений, которые необходимо произвести при допплеровском исследовании пациента с аортальной регургитацией.
Таблица 14. Параметры, определяемые при допплеровском исследовании пациента с аортальной регургитацией
Позиции и измерения 1. Наилучшего качества спектр струи аортальной регургитации из апикального доступа в 5-камерной позиции в постоянно-волновом режиме 2. Кровоток в нисходящей аорте из супрастернального доступа в импульсном режиме 3. Кровоток в брюшной аорте из субкостального доступа в импульсном режиме Расчетные параметры 1. Время полуспада диастолического градиента давления между аортой и левым желудочком 2. Отношение интегралов линейной скорости ретроградного и антероградного кровотока в нисходящем отделе аортыСкорость регургитирующей струи определяется разностью давлений между аортой и левым желудочком в каждый момент времени. Чем быстрее уменьшается скорость регургитирующей струи, тем быстрее выравнивается давление между аортой и левым желудочком, и, следовательно, тем тяжелее аортальная недостаточность (рис. 9.9). В предельно выраженных случаях скорость регургитирующей струи падает до нуля. Время полуспада диастолического градиента давления, (который с технической точки зрения этот параметр измеряется при аортальной регургитации так же, как при митральном стенозе) тем ниже, чем тяжелее аортальная недостаточность, то есть чем больше объем регургитирующей крови (рис. 9.10). Если T1/2 аортальной регургитации превышает 400 мс, то она почти наверняка легкой степени. Если T1/2 меньше 200 мс, то аортальная регургитация оценивается как тяжелая. Заметим, что время полуспада диастолического градиента давления между аортой и левым желудочком зависит от податливости аорты и левого желудочка, так что в определенных ситуациях использование этого параметра дает ошибку, например, при тяжелом поражении миокарда.
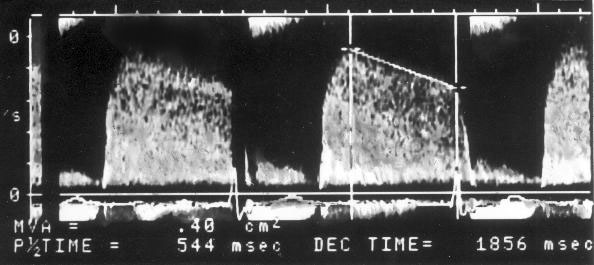
Рисунок 9.9. Аортальная регургитация: постоянно-волновое допплеровское исследование. Время полуспада градиента давления — 544 мс, что указывает на небольшую степень выраженности аортальной регургитации.
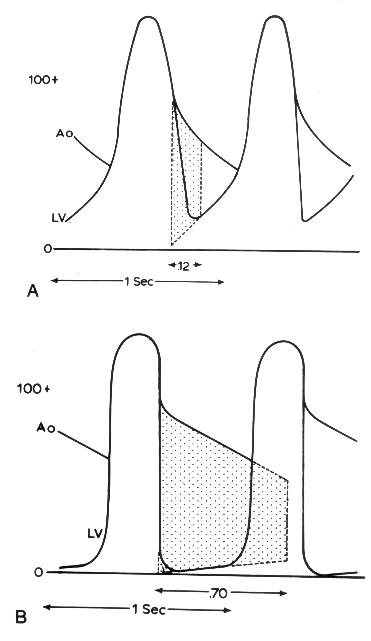
Рисунок 9.10. Кривые давления в аорте и в левом желудочке при тяжелой (А) и небольшой (В) аортальной недостаточности. Заштрихованная область соответствует времени полуспада градиента давления между левым желудочком и аортой. При тяжелой аортальной недостаточности давление в аорте в диастолу падает очень быстро, в левом желудочке так же быстро возрастает, поэтому происходит стремительное снижение градиента давления между желудочком и аортой. Время полуспада градиента давления в примере А — 120 мс. При небольшой аортальной недостаточности время полуспада градиента давления существенно больше: в примере В оно составляет 700 мс. Teague S.M. Doppler echocardiographic evaluation of aortic regurgitation, in: Doppler Echocardiography, ed. Schiller N.B., Cardiology Clinics, 8(2), 1990.
Иногда при сочетании аортальной недостаточности и митрального стеноза могут возникнуть трудности в различении их спектров. Струя аортальной регургитации отличается тем, что появляется в самом начале диастолы (когда митральный клапан еще закрыт) и начальная скорость ее — около 4 м/с. Что касается стенотической струи при митральном стенозе, по ее появлению предшествует период изоволюметрического расслабления левого желудочка, а начальная скорость ее — около 2 м/с (рис. 9.11). На правильность оценки тяжести аортальной регургитации по времени полуспада градиента давления между левым желудочком и аортой не влияет наличие митрального стеноза.
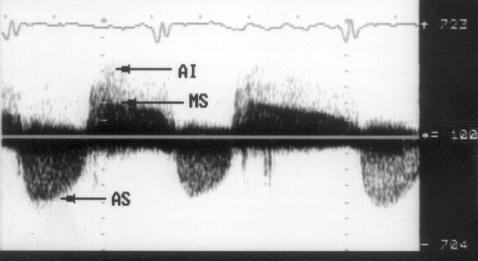
Рисунок 9.11. Регистрация струи аортальной регургитации и кровотока через стенозированный митральный клапан на одном допплеровском спектре. Постоянно-волновое допплеровское исследование из апикального доступа. Аортальная регургитация имеет большую скорость и начинается раньше — сразу после закрытия аортального клапана. Началу трансмитрального кровотока предшествует период изоволюметрического расслабления левого желудочка. AI — струя аортальной регургитации, MS — кровоток через стенозированный митральный клапан, AS — систолический кровоток через стенозированный аортальный клапан.
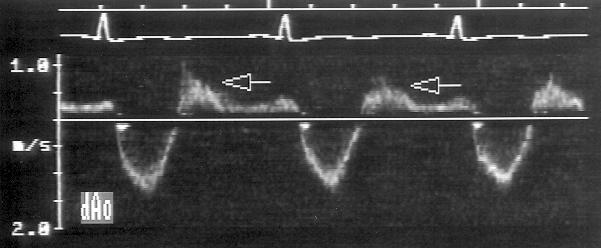
Если ретроградный (направленный к датчику, установленному в яремной ямке) диастолический кровоток в нисходящем отделе аорты не выявляется, то можно утверждать, что гемодинамически значимая аортальная регургитация отсутствует. Если же ретроградный кровоток обнаружен (рис. 9.12A), то можно сопоставить его объем с объемом антероградного кровотока — их соотношение хорошо коррелирует с фракцией регургитирующего объема, измеряемой при ангиографии [131]. Кроме того, объем регургитации можно измерить по разности систолического кровотока в выносящем тракте левого желудочка (повышенного) и в легочной артерии (нормального).
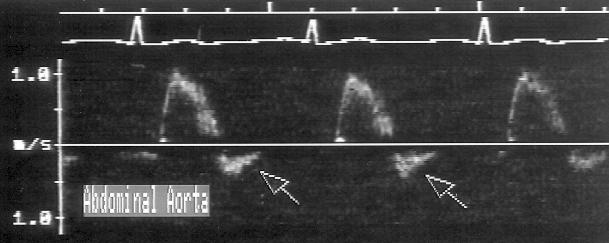
Ретроградный кровоток в брюшной аорте всегда указывает на тяжелую аортальную недостаточность (рис. 9.12B).
A
B
Рисунок 9.12. Ретроградный диастолический кровоток в нисходящем отделе аорты (стрелки) и в брюшной аорте. При исследовании нисходящей аорты (А) нормальный (антероградный) кровоток направлен от датчика (под изолинией), ретроградный кровоток — к датчику (над изолинией); при исследовании брюшной аорты (В) — наоборот. Ретроградный кровоток в брюшной аорте указывает на тяжелую аортальную недостаточность.
Определение этиологии аортальной недостаточности
Любой патологический процесс, затрагивающий аортальный клапан, может приводить к аортальной регургитации. Самая частая ее причина — дегенерация створок аортального клапана, наблюдающаяся при артериальной гипертонии и у пациентов пожилого возраста. Кальциноз и утолщение створок в наибольшей степени выражены на границе комиссур с аортальным кольцом. Кальциноз митрального и аортального колец часто сопровождает склерозирование створок аортального клапана. Иногда одна створок теряет свою подвижность, что хорошо заметно на фоне движения остальных. Если только одна из створок становится неподвижной, то это обычно не приводит к гемодинамически значимому аортальному стенозу, и аортальная регургитация при этом тоже, как правило, невелика.
Аортальная регургитация может быть ревматического происхождения. Края створок при этом утолщаются по всей длине, аортальное кольцо не вовлекается в патологический процесс и остаются нормальными. Как правило, при ревматизме обнаруживается аортальная регургитация легкой степени, но она может быть и умеренно выраженной, и даже тяжелой.
Двустворчатый нестенозированный аортальный клапан — еще одна нередкая причина аортальной регургитации. Вопрос об эхокардиографическом распознавании двустворчатого аортального рассмотрен выше (см. раздел «Определение этиологии аортального стеноза»). Аортальная регургитация при двустворчатом аортальном клапане, не пораженном бактериальным эндокардитом, обычно гемодинамически незначима.
Бактериальный эндокардит — ведущая причина тяжелой аортальной недостаточности. При классическом варианте бактериального эндокардита обнаруживаются вегетации — плотные, пролабирующие в левый желудочек эхо-структуры (рис. 16.15). Однако, как и в случаях поражения митрального клапана, примерно в 25% случаев клинически подтвержденного бактериального эндокардита вегетаций при эхокардиографическом исследовании не обнаруживается. Мешают диагностике предшествовавшие структурные изменения клапана, ставшие мишенью для инфекции. Абсцесс корня аорты — серьезное осложнение бактериального эндокардита. При абсцессе корня аорты в области синусов Вальсальвы появляется эхо-негативное пространство, являющееся полостью абсцесса (рис. 9.13, 16.19).

Рисунок 9.13. Абсцесс корня аорты: парастернальная длинная ось левого желудочка. Стрелкой отмечена полость абсцесса. Абсцесс корня аорты — осложнение бактериального эндокардита и самая частая причина аневризм синусов Вальсальвы. RV — правый желудочек, LV — левый желудочек, LA — левое предсердие, Ao — восходящий отдел аорты.
Аневризмы синусов Вальсальвы могут быть врожденными или приобретенными вследствие бактериального эндокардита; эхокардиографически это состояние проявляется несимметричным расширением корня аорты, выпячиванием дилатированного синуса в систолу. При аневризме синуса Вальсальвы тщательно проведенное допплеровское исследование может выявить и аортальную регургитацию, и внутрисердечный шунт.
Аортальная регургитация может присоединяться к субаортальному стенозу. Динамическая или фиксированная обструкция выносящего тракта левого желудочка иногда приводит к функциональной неполноценности аортального клапана из-за длительного воздействия на него стенотической струи.
Аортальная регургитация может появиться в результате миксоматозных изменений створок или как следствие поражения восходящего отдела аорты. Изредка диагностируется пролапс аортального клапана (рис. 9.14), сочетающийся с пролапсом митрального клапана. Синдром Марфана (и другие врожденные заболевания соединительной ткани) также проявляется пролапсом митрального клапана и аортальной недостаточностью. Для синдрома Марфана не характерен пролапс аортального клапана, но наблюдается изолированная дилатация синусов Вальсальвы и восходящего отдела аорты [94].
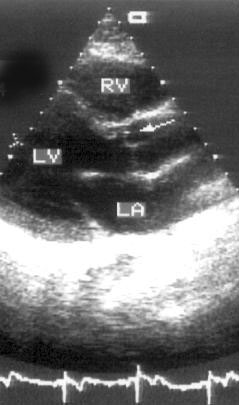
Рисунок 9.14. Пролапс аортального клапана: парастернальная длинная ось левого желудочка. Правая коронарная створка аортального клапана (стрелка) в диастолу пролабирует в полость левого желудочка. RV — правый желудочек, LV — левый желудочек, LA — левое предсердие.
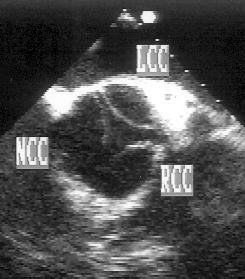
Аортальной регургитацией сопровождаются многие другие поражения аорты: проксимальное расслаивание аорты, аневризматическое расширение аорты при гипертонии, аорто-аннулярная эктазия (рис. 9.15), сифилитический мезаортит, расширение корня аорты при анкилозирующем спондилите. Эти заболевания не имеют специфических эхокардиографических признаков, их диагностика должна основываться на клинических признаках. Все перечисленные болезни сопровождаются расширением корня аорты и утолщением ее стенок.

A
B
Рисунок 9.15. Аорто-аннулярная эктазия. При трансторакальном исследовании (А) видна выраженная дилатация корня аорты и ее восходящего отдела. Расширенная аорта сдавливает правую легочную артерию. Максимальный диаметр аорты достигает 6 см. При чреспищеводном эхокардиографическом исследовании (В) обнаруживаются неизменный аортальный клапан, нормальные размеры дуги и нисходящего отдела аорты. RV — правый желудочек, LV — левый желудочек, LA — левое предсердие, Ao — восходящий отдел аорты, rPA — правая легочная артерия, LCC — левая коронарная створка аортального клапана, RCC — правая коронарная створка аортального клапана, NCC — некоронарная створка аортального клапана.
При расслаивающей аневризме аорты трансторакальная эхокардиография иногда выявляет отслойку интимы (рис. 9.16), но для диагностики этой патологии существенно большую ценность имеет чреспищеводное эхокардиографическое исследование.
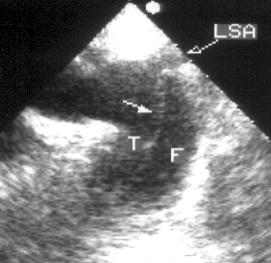
Рисунок 9.16. Расслаивающая аневризма аорты: длинная ось дуги аорты из супрастернального доступа. Расслаивание произошло дистальнее левой подключичной артерии. Как правило, для диагностики расслаивающей аневризмы аорты (особенно нисходящего отдела аорты) методом выбора является чреспищеводная эхокардиография, но иногда диагноз можно поставить и при трансторакальном исследовании. LSA — левая подключичная артерия, T — истинный канал, F — ложный канал, стрелкой указан отслоившийся участок интимы.
В редких случаях причиной аортальной регургитации может стать поражение клапана ревматоидными узелками, приводящими к появлению локальных участков уплотнения на створках. При подозрении на серьезную патологию восходящего отдела аорты, ее дуги или нисходящего отдела рекомендуется проведение чреспищеводной эхокардиографии. Патология брюшной аорты хорошо диагностируется при абдоминальном ультразвуковом исследовании (рис. 9.17, 2.20).
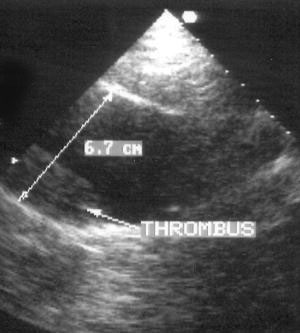
Рисунок 9.17. Аневризма брюшного отдела аорты: максимальный диаметр брюшной аорты составил 6,7 см. В полости аневризмы — пристеночный тромб.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Глава 32. Атаковать корень зла
Глава 32. Атаковать корень зла При встрече со всадником сначала стреляйте в лошадь, При встрече с разбойниками сначала захватите их главаря. Это знаменитые строчки Ду Фу, великого поэта царства Тан.Среди 36 стратагем, которые называются «популярным военным искусством»,
Глава 8. Митральный клапан
Глава 8. Митральный клапан Общие вопросыНормальные клапаны сердца так тонки и подвижны, что их не удается визуализировать с помощью большинства диагностических методов. Эхокардиография, которая фиксирует различия в акустических характеристиках между соединительной
Глава 10. Трехстворчатый клапан
Глава 10. Трехстворчатый клапан Эхокардиографическое изучение трехстворчатого клапана, технически более трудное, чем исследование митрального клапана, позволяет обнаружить как первичные его поражения, так и изменения, связанные с другой патологией сердца. Поэтому оно
Глава 11. Клапан легочной артерии
Глава 11. Клапан легочной артерии Легочная артерия и ее клапан визуализируются из нескольких эхокардиографических позиций. Лучше всего эти структуры видны при исследовании из парастернального доступа (рис. 2.6, 2.8). Иногда легочную артерию и ее клапан можно
Стеноз аорты
Стеноз аорты Стеноз аорты – врожденный порок, характеризующийся наличием препятствия току крови из левого желудочка в аорту в результате деформации створок клапана и (или) сужения клапанного кольца. Он наблюдается у 2-11 % детей, причем у мальчиков встречается в 3 раза
Коарктация аорты
Коарктация аорты Коарктация аорты (КА) – это врожденное сужение аорты на коротком ее участке (взрослый тип КА) или выраженное ее сужение на большом протяжении (инфантильный тип КА). Частота порока составляет 7,5-16 % от всех ВПС. Порок в 2–4 раза чаще встречается у мальчиков,
Коарктация аорты
Коарктация аорты Коарктация аорты — врожденное значительное сужение некоторой части аорты. Этот порок занимает четвертое по частоте место среди всех врожденных пороков сердца. Может наблюдаться как изолированно, так и в сочетании с другими пороками сердца. У мужчин
Аортальный стеноз
Аортальный стеноз Аортальный стеноз — это сужение входа в аорту. Самый большой сосуд организма человека — аорта выходит из левого желудочка. В фазе систолы левый желудочек под большим давлением выталкивает кровь в аорту. Для того чтобы в фазу диастолы, когда давление в
ЗАБОЛЕВАНИЯ АОРТЫ
ЗАБОЛЕВАНИЯ АОРТЫ Стенки аорты и артерий должны выдерживать скользящее воздействие толчка крови при каждом сокращении сердца. Имея большой диаметр, аорта испытывает значительно большее напряжение, чем другие отделы кровеносной системы, так как напряжение стенки прямо
Аконит (корень-борец, голубой лютик, иссык-кульский корень)
Аконит (корень-борец, голубой лютик, иссык-кульский корень) О ядовитых свойствах аконита люди знали с глубокой древности. Народные названия растения также соответствовали свойствам этого растения. Аконит называли и «волчья смерть» и «железный шлем», и
КОАРКТАЦИЯ АОРТЫ
КОАРКТАЦИЯ АОРТЫ Порок представляет собой врожденное сужение аорты на ограниченном участке, располагающееся несколько дистальнее места отхождения левой подключичной артерии. На аорте обнаруживается перетяжка, внутренняя сторона которой подтянута медиально. Степень
Глава 25. КОРЕНЬ БОЛИ
Глава 25. КОРЕНЬ БОЛИ Причины, породившие боль, могут быть самыми разными. Но каковы бы ни были болевые проявления, их роднит одно обстоятельство — присутствие корня боли.Когда боль появляется, она еще не имеет глубинной основы в тканях и органах. Она возникает как
Аневризма аорты
Аневризма аорты Аневризма аорты представляет собой локальное растяжение или выпячивание ее стенки. В зависимости от локализации выделяют аневризму восходящей аорты, аневризму дуги, аневризму нисходящей аорты, аневризму брюшной аорты, торакоабдоминальную
Аневризма аорты
Аневризма аорты Аневризма аорты представляет собой локальное растяжение ее стенки. Причиной возникновения аневризмы может быть атеросклероз аорты, врожденный дефект стенки аорты, инфекции или травмы. Симптоматика заболевания различна. Основным симптомом являются
Аневризма аорты
Аневризма аорты При прорыве расслаивающейся аневризмы аорты в трахею или бронхи возникает профузное легочное кровотечение. При незначительном надрыве стенки аорты отмечаются умеренные повторные легочные кровотечения, служащие предвестниками окончательного прорыва
Глава 1 ЗРИ В КОРЕНЬ! ВОЗМОЖНЫЕ ПРИЧИНЫ ВЫПАДЕНИЯ
Глава 1 ЗРИ В КОРЕНЬ! ВОЗМОЖНЫЕ ПРИЧИНЫ ВЫПАДЕНИЯ Нет ни малейшего сомнения в том, что самой заметной проблемой, связанной с волосами, является их выпадение. Оно принимает различные формы и может быть вызвано различными причинами. На языке медиков выпадение волос принято