Интенсивная терапия сепсиса
Интенсивная терапия сепсиса
В настоящее время сепсис продолжает оставаться одной из наиболее важных общебиологических проблем. Сформировавшееся еще в начале прошлого столетия представление о сепсисе в последние два десятилетия претерпело серьезные изменения. На сегодняшний день сепсис определяют как системную реакцию на инфекцию. В центре внимания врача находится не возбудитель, а вызванная бактериальным токсином избыточная воспалительная реакция организма. В связи с этим принципиально изменился и подход к лечению сепсиса. В Германии смертность от сепсиса за год составляет свыше 75 000 случаев (равна таковой от инфаркта миокарда). В целом в Европе ежегодно регистрируется до 500 000 случаев сепсиса – один на тысячу госпитализируемых. Примерно такие же ситуации в США. Летальность при сепсисе остается очень высокой, достигая 50% случаев. Смертность у больных грамотрицательным сепсисом в два раза выше летальности больных сепсисом, вызванным грамположительной флорой. Наиболее высокая летальность, достигающая 80–90%, описывается в группах пациентов с полиорганной недостаточностью. После проведения многоцентрового эпидемиологического когортного проспективного исследования включившего 14 364 пациента в 28 ОРИТ Европы, Израиля и Канады выяснено, что на пациентов с сепсисом приходится 17,4% от группы больных прошедших этап интенсивного лечения причем 63,2% из них явилось осложнением госпитальной инфекции. В результате тщательных эпидемиологических исследований завершенных в 2003 году в странах Европы (EPISEPSIS) и Австралии (ANZICS), эксперты пришли к заключению, что частота сепсиса в индустриально развитых странах составляет 50–100 случаев на 100 000 населения.
Доказано, что в группе микробиологически верифицированных инфекций самая высокая летальность обусловлена грамотрицательными бактериями и грибами. Однако, микробиологическое подтверждение возможно менее чем в половине случаев сепсиса, а установление спектра возбудителей и их резистентности невозможно совсем или растянуто по времени. Поэтому, лечебная тактика инфекционных поражений, особенно в начале лечения, основывается на клинически проявляющихся синдромах.
Проблема заключается еще и в том, что вплоть до сегодняшнего дня отсутствует единое определение сепсиса. Общим является только наличие очага инфекции. Понятия септицемии, бактериемии и сепсиса нередко используют как взаимозаменяемые. Бактериемию часто путают с септицемией, т. е. обнаружение возбудителей в гемокультуре одновременно с симптомами сепсиса. В результате подобного некритического использования понятий возможна недооценка частоты возникновения сепсиса, так как более чем в половине всех случаев сепсиса возбудители в крови вообще не обнаруживают.
Даже микробиологический спектр сепсиса изучен недостаточно. Недостаточно эффективна также терапия сепсиса, сопровождающаяся летальностью более 40 %. Высокая летальность зависит, по крайней мере частично, от микробиологических триггеров, таких как эндотоксины грамотрицательных бактерий, вызывающих активацию каскада цитокинов с повреждающим функциональным действием. Увеличилось количество случаев сепсиса возникающего в результате активации «оппортунистической» микрофлоры. Стало очевидным, что проблема лечения сепсиса не решается только с помощью антибактериальной терапии. Поэтому в связи с таким представлением о патогенезе сепсиса возник вопрос: может ли нейтрализация токсинов и/или модуляция воспалительных реакций, антицитокиновыми препаратами или с помощью иммуноглобулинов, по возможности снизить летальность при сепсисе.
Произошедшее в последние годы существенное изменение трактовки этиопатогенеза сепсиса, господствующее с начала XX века до недавнего времени, затронуло также и его терапию.
Понятие сепсиса
Классическое определение сепсиса было разработано еще в начале хх века. Тогда сепсис представляли как наличие в организме очага инфекции, из которого в кровяное русло попадают патогенные возбудители. В результате этого вторжения и возникают проявления болезни. Это классическое определение сепсиса, от которого отдельные исследователи не отказались и сегодня, оказалось малополезным для эффективного клинического применения.
Пытаясь максимально минимизировать существующие противоречия в понимании патогенеза сепсиса, обозначить различающиеся по тяжести клинического течения его формы, консенсусная конференция общества критической медицины и торакальных врачей (США) предложила схему, представленную в табл. 1. Согласно решению конференции, определение сепсиса основывается только на клинических критериях и не требует обязательного обнаружения возбудителей в гемокультуре. Сепсис воспринимается как системная реакция на инфекцию. Он выражается в виде тахикардии, тахипноэ, изменения температуры и лейкоцитоза или лейкоцитопении. Тяжелый сепсис (или септический синдром) имеется тогда, когда сепсис отягощается признаками дисфункции органов, такими как лактат-ацидоз, олигурия, гипоксемия или изменение сознания. Септический шок определяют как тяжелый сепсис, сочетающийся с рефрактерной к инфузионной терапии гипотонией.
Напоминающая бактериальный сепсис картина может возникнуть и без наличия первичной микробной инфекции. В этих случаях возникает идентичная картина болезни и ее течения как вследствие микробной инфекции, так и в результате первично- неинфекционных причин, таких как травма,ожоги, панкреатит или интоксикация. Если в определении иметь в виду неинфекционные причины, то этот синдром предлагается обозначить как синдром системного воспалительного ответа (SIRS) (см. таблицу 1). В качестве связующего звена между микробным сепсисом и немикробным SIRS, (systemic inflammatory response syndrome) предположительно может явиться феномен транслокации бактерий и эндотоксина из кишечника вследствие ишемии кишечника в ходе общего воспалительного процесса. Каждое определение сепсиса только весьма ограниченно отражает многообразие клинической реальности. Поэтому и предлагаемое американскими врачами определение сепсиса, тяжелого сепсиса и септического шока не может полностью охватить широкий спектр всех клинических симптомов и всех изменений лабораторных показателей при сепсисе. Но все же это важный шаг к общему клиническому пониманию сепсиса, дающий нам возможность двигаться дальше в сторону решения этой важной проблемы в практическом и теоретическом направлениях.
Таблица 1. Определение сепсиса согласно конференции по консенсусу ACCP/SCCM
Инфекция - микробный феномен, характеризуется воспалительной ре-акцией на наличие микроорганизмов или на проникновение этих организмов в обычно стерильную ткань.
Бактериемия - наличие живых бактерий в крови.
Синдром системного воспалительного ответа (SIRS) - системная воспалительная реакция на одну из множества тяжелых клинических причин (инфекция, панкреатит, повреждение тканей, травма, ишемия, экзогенное введение воспалительных медиаторов, таких как а – ФНО). Реакция манифестирует в виде возникновения двух или более признаков: температура выше 38° С или гипотермия ниже 36° С; тахикардия (ЧСС более 90 в минуту); тахипноэ (ЧД более 20 в минуту или раСО2 менее 32 мм рт. ст.); лейкоциты более 12 000 в 1 мкл, или менее 4000 в 1 мкл, или незрелые формы более 10 %.
Сепсис - системная реакция на инфекцию. Реакция манифестирует в виде двух или более признаков: темп. выше 38°С или гипотермия ниже 36°С; тахикардия (ЧСС более 90 в минуту); тахипноэ (ЧД более 20 в минуту или раСО2 менее 32 мм рт.ст.); лейкоциты более 12 000 в 1 мкл, или менее 4000 в 1 мкл или незрелые формы более 10 %.
Тяжелый сепсис - сепсис, связанный с дисфункцией органов, нарушением перфузии или гипотонией; нарушения перфузии могут включать возникновение лактат-ацидоза, олигурии или острого изменения ментального статуса, но не ограничиваются перечисленными; гипотония определяется как систолическое кровяное давление менее 90 мм. рт. ст. или снижение систолического давления более 40 мм. рт . ст. при отсутствии других причин гипотонии.
Септический шок - сепсис с гипотонией (см. выше), несмотря на адекватное возмещение объема вместе с нарушением перфузии, включающей появление лактат-ацидоза, олигурии или острого изменения ментального статуса, но не ограничиваются эти-ми. Пациенты при терапии сосудосуживающими или ноотропными агентами могут также не быть гипотоническими, если имеются нарушения перфузии.
Синдром полиорганной дисфункции - измененная функция органов у пациента с острой формой болезни такого рода, что без вмешательства гемостаз поддерживаться не может.
Патофизиология сепсиса
Таким образом, в основе понимания патофизиологии сепсиса сегодня находится не возбудитель, а вызванная бактериальным токсином чрезмерная воспалительная реакция организма. В настоящее время полагают, что именно гипервоспалительная реакция иммунной системы способствует развитию септического шока и поражению органов (легкие, печень, почки, сердце).
Как правило, инфекция может проявляться тогда, когда микроорганизмы проникают через или обходят такие барьеры организма, как кожа или слизистые оболочки. Токсические бактериальные продукты попадают в циркуляцию, после чего активируют системные защитные механизмы, к которым относятся система комплемента и каскад свертывания, а также клеточные компоненты крови: нейтрофилы, моноциты, макрофаги и клетки эндотелия. Активированные клетки продуцируют медиаторы, которые инициируют и поддерживают воспалительную реакцию. К таким медиаторам относятся цитокины (фактор некроза опухоли – ФНО), интерлейкин-1 (ИЛ-1. и др., кинины, метаболиты арахидоновой кислоты, фактор активации тромбоцитов и оксид азота (табл. 2). Гипервоспалительная реакция организма (SIRS) может вместе с микробными токсинами привести к повреждению клеток, нарушению перфузии и в итоге к шоку, полиорганной недостаточности и смерти. Провоспалительные цитокины играют защитную роль, поскольку обеспечивают рекрутирование в очаг инфекции дополнительное количество эффекторных клеток (нейтрофилов, макрофагов), стимулируют их фагоцитарную, бактерицидную активность и индуцируют запуск антигенспецифического ответа, что в совокупности способствует элиминации патогена. Эффективность этого процесса определяется его адекватностью.
Следует отметить, что защитная роль провоспалительных цитокинов рационально проявляется тогда, когда эти медиаторы работают локально, в очаге воспаления, однако их системная продукция вовсе не означает высокую эффективность противоинфекционного иммунитета. Напротив, избыточная и генерализованная продукция провоспалительных цитокинов приводит к развитию бактериально-токсического шока и органных дисфункций, что может явиться причиной летального исхода на ранних этапах септического процесса (табл.3).
Для избежания избыточных проявлений системного воспаления вслед за SIRS в организме включаются механизмы негативного контроля, опосредованные продукцией противовоспалительных цитокинов и растворимых ингибиторов провоспалительных цитокинов. Для обозначения данного состояния R. Bone в 1996 г. предложил использовать акроним CARS, или синдром компенсаторного противовоспалительного ответа (compensatory anti-inflammatory response syndrome) (рис. 1).C A R S
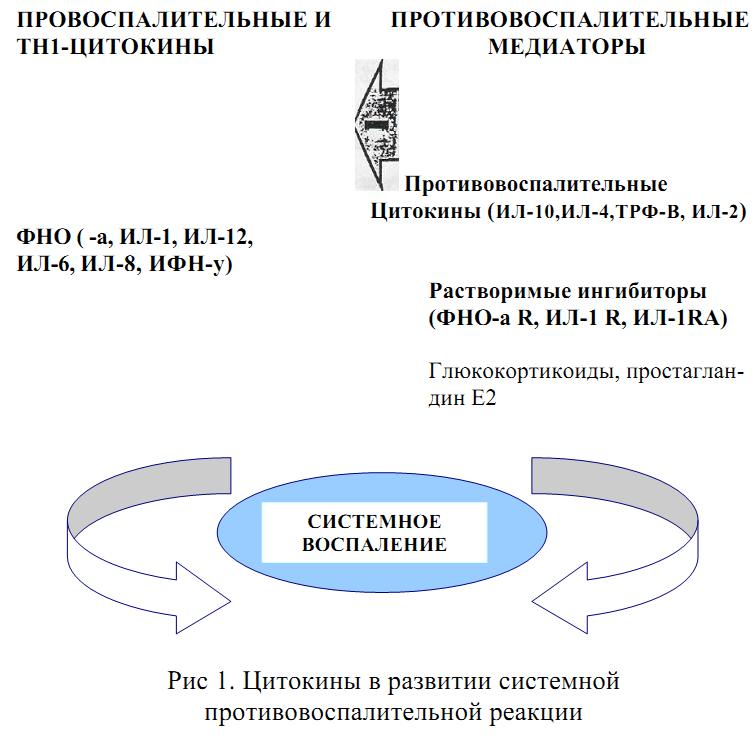
При сбалансированном течении CARS подавляет системную воспалительную реакцию и приводит к восстановлению гомеостаза. При чрезмерной выраженности или пролонгированном течении CARS вызывает развитие глубокой иммунодепрессии, что обычно клинически проявляется хронизацией или диссеминацией инфекции, присоединением нозокомиальной микрофлоры, нарушением процессов репарации, утяжелением эндотоксикоза и формированием поздней полиорганной недостаточности, что в совокупности предопределяет летальный исход.
Основой патогенеза сепсиса является запуск цитокинового каскада, который включает, с одной стороны, провоспалительные цитокины, а с другой – противовоспалительные медиаторы. Баланс между этими двумя разнонаправленными по действию группами во многом определяет характер течения и исход сепсиса. В связи с этим управление цитокиновым балансом можно рассматривать в настоящее время как новую мишень терапевтических воздействий при лечении гнойно – септических заболеваний. Совершенно очевидно, что противовоспалительная, например, антицитокиновая терапия оправдана только в случае крайней выраженности системного воспалительного ответа, а при несбалансированном течении CARS показано применение препаратов с противоспалительной активностью, среди которых наиболее перспективным представляется использование Th 1 – цитокинов (ИЛ-1, ИЛ-12, или ИЛ-2, ИФН-гамма). Как известно, цитокины этой группы, наряду с усилением неспецифических механизмов про- тивоинфекционной защиты, эффективно стимулируют развитие специфического иммунного ответа и активируют репаративные процессы в поврежденных тканях. Кроме того, являясь функционально активными иммунорегуляторными факторами, цитокины не требуют значительного интервала времени для реализации своего эффекта, что чрезвычайно важно при оказании неотложной медицинской помощи.
Значение эндотоксина при сепсисе
Примерно почти в половине случаев, в которых удается микро-биологически выделить возбудителя при сепсисе, вызывающие его микроорганизмы оказываются грамотрицательными бактериями. Чаще всего это E. Coli, Klebsiella spp., Enterobacter spp., Seratia spp., Pseudomonas aeruginosa и Proteus spp.
При грамотрицательном возбудителе сепсиса центральную патогенетическую роль триггера играет бактериальный эндотоксин (липополисахарид – ЛПС).
Бактериальный эндотоксин является компонентом клеточной стенки грамотрицательных бактерий. Эндотоксины отдельных видов грамотрицательных бактерий, хотя и различны в деталях, но имеют общую структуру: антигенные сахаридные цепи привязаны к гидрофобному липиду А, который и обладает собственно повреждающим действием. Общая структура и ее локализация на стенке бактериальной клетки приводит к тому, что эндотоксин распознается иммунной системой. Распознавание антигена является одновременно также фактором запуска каскада медиаторов и высвобождения проявляющих повреждающее действие цитокинов.
Эндотоксин высвобождается в процессе гибели микроорганизмов, вызванной антибиотиками, комплементом или фагоцитозом. В эксперименте на морских свинках было показано, что индуцированное гентамицином высвобождение эндотоксина отрицательным образом сказывается на сердечном выбросе и давлении в легочной артерии. Аналогичным образом терапия антибиотиками индуцировала в модели на кроликах при: грамотрицательном менингите – подъем эндотоксина в ликворе и ассоциативное увеличение церебрального отека.
Таблица 2.
1. Инфекционный очаг (Абсцесс, пневмония, перитонит, пиелонефрит)
2. Внедрение микроорганизмов и токсинов
3. Микроорганизмы
• Грамотрицательные бактерии
• Грамположительные бактерии грибы
4. Токсины
Эндотоксины, экзотоксины, Teichoic-acid-антиген (антиген тейхоевых кислот)
5. Активация иммунной системы
• Гуморальная система: система комплемента, система свертывания, брадикинин
• Клеточная система: макрофаги, моноциты, гранулоциты, клетки эндотелия
6. Высвобождение медиаторов
• Цитокины, (ФНО, ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-10 и др.)
• Комплемент (С3а, С5а)
• Фактор свертывания (фактор Хагемана)
• кинины (брадикинин)
• липидные метаболиты (лейкотриены, простагландины)
• протеазы (эластаза, коллагеназа)
• токсические кислородные продукты (супероксиды Н2О2, ОН)
• оксид азота (NO)
• протеины адгезии (селектины, ICAMs, CD 11/18)
7. Повреждение клеток и нарушение перфузии
8. Шок и полиорганная недостаточность
Огромным резервуаром эндотоксина является кишечник. Пред-полагается, что разрушение барьера слизистой желудочно-кишечного тракта может без бактериемии привести к эндотоксинемии.
В условиях гипоперфузии слизистой кишечника, нарушения пищеварения, инфекции или абдоминальных хирургических вмешательств эндотоксин может проникать в систему кровообращения и одновременно с транслокацией бактерий кишечника. Правда, в на-стоящее время этот процесс не представляется таким однозначным и требует дальнейшего изучения.
Эндотоксинемия и грамотрицательная бактериемия осложняют течение основного заболевания, усиливают эффекты экзотоксинов, обусловливают полиорганную недостаточность. Эндотоксин связывается при посредстве ЛПС-связывающего протеина с CD14 рецепторами макрофагов и полиморфноядерных гранулоцитов, являясь триггером ответственной реакции хозяина на нагрузку эндотоксином. От этого решающим образом зависит, будет ли возбудитель элиминирован или реакция окажет повреждающее действие на организм-хозяин, вплоть до формирования полиорганной недостаточности. Клинически эта реакция проявляется как сепсис.
Возможности диагностики.
Совершенно очевидно, что определение в крови эндотоксина может свидетельствовать о генерализации инфекционного процесса. Используемый для этого самый чувствительный метод – лимулюс амебоцитный лизатный тест (ЛАЛ – тест). Он основывается на открытии того, что у рачка Limulus polyphemus инъекция грамотрицательных бактерий ведет к диссеминированному внутрисосудистому свертыванию. Исследования показали, что свертывание гемолимфы обусловливает один компонент бактерии – эндотоксин. Чтобы вызвать этот эффект, достаточно 1 пг очищенного эндотоксина. Нужные для активации процессов свертывания факторы можно найти в гранулах, имеющихся в специализированных кровяных клетках рачка Limulus polyphemus – амебоцитах. С применением лизата этих клеток разработан простой тест свертывания для измерения количества эндотоксина. Присутствие эндотоксина вызывает каскадную реакцию в клетках, в которой участвуют три протеазы. Эта реакция активизирует энзим, который расщепляет клеточный протеин на 3 полипептидные цепочки, 2 из этих цепочек отвечают за гелирование лимфы. Этот процесс полностью аналогичен человеческому каскаду свертывания. В лаборатории содержание эндотоксина определяется фотометрически, путем добавления к энзиму хромогенного субстрата, в качестве которого используют связанный с дипептидом n-нитроанилин. Цветная реакция происходит, если энзим отщепляет фрагмент n-нитроанилина.
Показано, что определяемые очень низкие концентрации эндотоксина порядка 10 пг/мл в плазме могут свидетельствовать о грамотрицательном сепсисе. Результаты исследований показали, что наличие и уровень эндотоксинемии коррелируют с клиническим исходом. Исследователи полагают, что этот тест можно использовать при сепсисе для оценки прогноза. Выявлено, что начальные концентрации в плазме ‹ 25, 25 – 700, 700 – 10 000 пг/мл и › 10 000 пг/мл кореллируют, соответственно, с летальностью 0, 14, 27 и 86 %. При этом титр эндотоксина более 700 пг/мл статистически достоверно соответствует развитию шока.
Однако ряд фактов осложняет интерпретацию концентрации эндотоксина в плазме. Различные грамотрицательные бактерии имеют неодинаковое количество ЛПС и высвобождают различные количества эндотоксина в результате отторжения фрагментов клеточной мембраны во время фазы роста. Последняя особенность четко обозначена у менингококковых штаммов. Кроме того, эндотоксины различных грамотрицательных бактерий имеют различную активность по отношению к тесту, что не всегда коррелирует с биологическим действием. Это означает, что абсолютные концентрации не всегда точно отражают степени тяжести грамотрицательного сепсиса. Обнаружение концентраций эндотоксина в плазме может быть использовано для ранней индикации развития сепсиса. Отрицательный результат не исключает, что эндотоксины и медиаторы уже оказали свое действие и в крови больше не обнаруживаются. Часто эндотоксин при самом тяжелом сепсисе обнаруживается в циркуляторном русле только в течение короткого времени.
Несмотря на это, при обнаружении эндотоксина в человеческой плазме хромогенный ЛАЛ-тест оказывается единственным клинически практикуемым методом индикации и количественной оценки эндотоксина в плазме.
В клинической практике для оценки эндотоксикоза применяется целый ряд методов, позволяющих косвенно судить о его тяжести. Существуют специальные методы индикации токсичных веществ, определяющих степень эндотоксикоза. К ним относят биотестирование на мышах, резистентность у которых снижается предварительной блокадой ретикулоэндотелиальной системы; метод гемокультуры, основанный на изменении свойств лейкоцитов под действием токсина; метод определения токсичности плазмы с помощью реакции, которая основана на гибели парамеций (простейших класса инфузорий) под влиянием токсического фактора; лейкоцитарный индекс интоксикации; метод определения уровня средних молекул. Им придается определяющая роль в формировании эндотоксемии и сепсиса. В последние годы для диагностики сепсиса и эндотоксикоза предлагается определение уровня прокальцитонина. Однако, к сожалению, все предлагаемые методы носят только вспомогательный характер и не имеют самостоятельного значения для диагностики сепсиса.
Эндотоксин – центральный инициатор сепсиса
Постулирование центральной роли эндотоксина при сепсисе возможно только при следующих условиях:
1. Уровень эндотоксина должен быть определяем при сепсисе.
2. Введение эндотоксина экспериментальным животным должно вызвать развитие состояния, подобное сепсису.
3. Нейтрализация эндотоксина должна положительным образом воздействовать на течение сепсиса и его исходы.
Имеющиеся в литературе исследования свидетельствуют о наличии эндотоксинов в крови у значительного числа септических пациентов, причем, эндотоксинемия коррелирует с развитием почечной недостаточности и респираторного дистресс-синдрома. Однако эндотоксин не всегда имеется в циркуляторном русле при сепсисе, но уровень его в случаях обнаружения всегда коррелирует с тяжестью клинической манифестации и проявлением полиорганной недоста-точности.
Все это дает возможность предположить, что эндотоксин, вероятно, не один инициатор сепсиса. Хорошо известно, что грамположительные и грибковые инфекции клинически могут протекать как грамотрицательный сепсис. Поэтому логично предположить, что в развитии сепсиса в роли триггера выступает множество других факторов, причем, эндотоксин является важнейшим. Таким образом, если эндотоксин является центральным триггером сепсиса, то введение его должно вызвать сходный с сепсисом синдром. После введения эндотоксина экспериментальным животным получены тяжелые патофизиологические изменения. Причем, они зависит от вида бактерий, дозы, способа введения, источника, из которого получен эндотоксин. Характерной реакцией являются вазодилатация, снижение сердечного выброса и развитие гипотензии.
Определяющим доказательством для выяснения непосредствен-ной роли эндотоксина могла бы явиться демонстрация клинического улучшения при нейтрализации или элиминация эндотоксина при клиническом сепсисе. Логичное решение задачи – пассивная иммунизация антителами против эндотоксина. Однако применение моноклональных антител против липида А не привело к клиническому результату. Применяемые в этих исследованиях антиэндоксинные антитела HA-IA и Е5 не нейтрализовали его эффекты.
По-видимому, эндотоксин является достаточным, но не единственным фактором инициирования сепсиса, а его роль должна быть уточнена.
Терапия сепсиса
Концептуальная смена патофизиологического понимания септического синдрома находит свое отражение также в изменении терапевтического подхода, который теперь, помимо антимикробных мер, включает иммунную модуляцию разрегулированных защитных реакций.
К стандартной стратегии терапии сепсиса относятся раннее введение антибиотиков, хирургическое вмешательство для санирования очага инфекции, ранняя инфузионная и детоксикационная терапия (диализ, плазмаферез, гемосорбция, механическая вентиляция) и использование вазоактивных медикаментов.
Повышенная частота возникновения сепсиса и высокая летальность привели к интенсивному поиску новых методов лечения. Разработка новых агентов для терапии сепсиса основывалась частично на положении, что нейтрализация бактериальных токсинов или потенциально повреждающих медиаторов иммунной системы может остановить септический процесс или, по крайней мере, замедлить его (табл. 3). Эти новые виды терапии направлены против различных элементов гипервоспалительного каскада, таких как ФНО и ИЛ- 1,оказались неэффективными. По крайней мере, на данном этапе изучения разработки клиническое его преломление не принесло позитивных результатов.
Европейские Рекомендации для Управления Тяжелым Сепсисом и Септическим Шоком
30 марта 2004г.
Компания по Выживанию при Сепсисе (The Surviving Sepsis Cam-paign – SSC) рада обеспечить Вас этой копией Рекомендаций. Эти рекомендации появятся в мартовском выпуске журнала Критической Медицины (March issue of Critical Care).
Диагностика
Соответствующие образцы крови всегда должны быть получены прежде, чем начата антимикробная терапия. Чтобы оптимизировать идентификацию болезнетворных микроорганизмов, по крайней мере, два образца крови для микробиологического исследования должны быть получены. Один из них, по крайней мере, следует получить при чрезкожной пункции сосуда (вены) и второй – через каждый сосудистый катетер, за исключением тех, которые были недавно (‹ 48 часов) установлены. Образцы из других местообитаний, типа мочи, цереброспинальной жидкости, раны, секреции из дыхательных путей или других жидкостей организма должны быть получены прежде, чем начата терапия антибактериальными препаратами, которые диктует клиническая ситуация. Антимикробный режим должен всегда пере-оцениваться после 48 до 72 часов на основе микробиологических и клинических данных с целью использования узко – спектрального антибиотика, чтобы предотвратить развитие устойчивости, уменьшить плотность токсичности, и уменьшить затраты. Как только причинный патогенетический микроорганизм идентифицирован, не имеется ни-каких доказательств, что комбинированная терапия является более эффективной, чем монотерапия. Продолжительность терапии должна обычно быть от 7 до 10 дней и управляться клиническим ответом.
Начальное восстановление
Восстановление пациента при тяжелом сепсисе или индуцированной сепсисом недостаточной перфузии ткани (гипотензия или лактат – ацидоз) должно начаться немедленно, как только синдром диагностирован, и не должно быть отсрочено, ожидая поступления в ОИТР. Повышенный плазменный уровень лактата идентифицирует недостаточную перфузию ткани у пациента высокого риска, который еще не гипотензивен.
В течение первых 6 часов восстановления целями реставрации индуцированной сепсисом недостаточной перфузии тканей должны быть все следующие параметры, как единая часть лечебного протокола:
1. Центральное венозное давление (ЦВД, CVP) 8–12 mmHg
2. Среднее артериальное давление (САД, МАР) › 65 mmHg
3. Диурез › 0.5 мл / кг час-1 Управление очагом инфекции
Каждый пациент с тяжелым сепсисом, септическим шоком дол-жен быть оценен на присутствие фокуса инфекции, подлежащей специальным мероприятиям санации очага (дренированию абсцесса или локального фокуса инфекции, хирургической обработке инфицированной раны, некротической ткани, удаление потенциально инфици-рованного устройства или оперативное определение источника, продолжающего бактериальное обсеменение.
Жидкостная терапия
Жидкостное возмещение при восстановлении пациента может состоять из естественных или искусственных коллоидов или кристаллоидов. Не имеется никакой доказательно – обоснованной поддержки для одного типа жидкости в противовес другому.
Хотя только предполагаемых (prospective) изучений выбора режима жидкостного возмещения при восстановлении у пациентов с септическим шоком недостаточно, мета-анализ клинических изучений, сравнивающий кристаллоиды и коллоиды при восстановлении в общих и хирургических популяциях пациентов, не указывает на какую – либо клиническую разность результата между коллоидами и кристаллоидами и, кажется, могли бы быть распространены на всю септическую популяцию. Поскольку объем распространения кристаллоидов намного больший, чем для коллоидов, восстановление с кристаллоидами требует большего количества жидкости, чтобы достичь тех же конечных результатов и приводит к большему количеству отеков.
Введение большого количества жидкости, способствующей восстановлению выделения (fluid challenge) у пациентов с подозрением на гиповолемию (подозрением на неадекватную артериальную циркуляцию) можно осуществлять со скоростью (темпом) 500–1000 мл кристаллоидов или 300–500 мл коллоидов в течение 30 минут и повторить, основываясь на ответе организма (увеличение кровяного давления и диуреза) и толерантности (доказательства внутрисосудистой перегрузки объемом).
Vasopressors
Когда соответствующее жидкостное возмещение при восстановлении (fluid challenge) недостаточно для восстановления адекватного кровяного давления и органной перфузии, терапия с вазопрессорными средствами должна быть начата. Вазопрессорная терапия может также потребоваться срочно, чтобы удержать жизнь и поддерживать перфузию на фоне жизнеугрожающей гипотензии (life- threatening hypotension), даже когда соответствующее жидкостное возмещение продолжается и гиповолемия еще не до конца скорректирована.
Dobutamine – инотропный препарат первого выбора (first-choice inotrope) для пациентов с измеренным или подозреваемым низким сердечным выбросом в присутствии адекватного левожелудочкового давления наполнения (или клинической оценки адекватности жидкостного возмещения при восстановлении) и адекватного среднего артериального давления. При отсутствии измерений сердечного выброса гипотензивные пациенты с тяжелым сепсисом могут иметь низкий, нормальный или увеличенный сердечный выброс. Поэтому рекомендуется лечение смешанным inotrope/vasopressor типа norepinephrine или dopamine. Когда существует возможность для мониторинга (контроля) сердечного выброса в дополнение к кровяному давлению, вазопрессор типа norepinephrine и inotrope, типа dobutamine, могут ис-пользоваться раздельно, достигая определенных целей по уровням среднего артериального давления и сердечного выброса.
Стратегия увеличивающегося сердечного индекса, чтобы достичь произвольно предопределенного повышенного уровня, не рекомендуется.
Стероиды
Внутривенные кортикостероиды (гидрокортизон 200–300 мг / день, в течение 7 дней в дозах, разделенных на 3 или 4 приема или в виде непрерывной инфузии) рекомендуются для пациентов с септическим шоком которые, несмотря на адекватное жидкостное возмещение при восстановлении, требуют, чтобы вазопрессорная терапия поддержала адекватное кровяное давление.
Одно мультицентровое, рандомизированное, контролируемое испытание (randomized, controlled trial -RCT) пациентов с тяжелым сепсисом и септическим шоком показало существенное влияние на обратное развитие шока и снижение смертности у пациентов с относительной надпочечниковой недостаточностью (определенной как пост – ACTH Cortisol повышение ‹ 9^g/dl) [39]. Два дополнительных меньших RCTS показали существенное влияние на обратное развитие шока (significant effects on shock reversal)]. В первом изучении пациенты имели более тяжелый септический шок (систолическое кровяное давление [SBP] ‹ 90 mmHg, несмотря на vasopressors), чем в последних двух изучениях (SBP › 90 mmHg с vasopressors).
Некоторые эксперты использовали 250 ^g ACTH для стимуляции, чтобы определить ответ организма (› 9 ^g /dl) на повышение cortisol 30–60 мин спустя после введения ACTH) и прекращать терапию у этих пациентов. Клиницисты не должны ждать результаты стимуляции адренокортикотропным гормоном, чтобы вводить кортикостероид. Одно изучение продемонстрировало, что постепенно возрастающее увеличение › 9 ^g /dl после 250 ^g ACTH стимулирующего теста (отвечающие организмы) идентифицирует оставшихся в живых пациентов с тяжелым сепсисом, или септическим шоком. Последующее испытание продемонстрировало, что стресс – доза стероидов улучшает выживание тех пациентов, которые не сумели показать повышение cortisol после стимуляции адренокортикотропным гормоном (неотвечающие организмы). Лечение кортикостероидами было неэффективно у отвечающих организмов. Рекомендации для идентификации относительной надпочечниковой недостаточности изменяются, основываясь на различных прерывистых, случайных уровнях cortisol, пиках cortisol после стимуляции, постепенно возрастающем увеличении cortisol после стимуляции, и комбинаций этих критериев. У пациентов с септическим шоком клиницисты должны рассмотреть введение дозы dexamethasone до того времени, как ACTH стимулирующий тест может быть проведен, потому что dexamethasone, в отличие от гидрокортизона, не требует количественного анализа cortisol. Дозы кортикостероидов выше чем ›300 мг гидрокортизона, ежедневно не должны использоваться при тяжелом сепсисе, или септическом шоке с целью их лечения. При отсутствии шока кортикостероиды не должны использоваться для лечения сепсиса.
Рекомбинантный активировнный белок C (Recombinant activated protein C – rhAPC). RhAPC рекомендуется пациентам с высокой степени риска смерти (APACHE II › 25, сепсис – индуцированная полиорганная недостаточность, септический шок или сепсис – индуцированный ARDS) и нет абсолютных противопоказаний (риск кровотечения) или относительных противопоказаний, которые бы перевешивали потенциальный успех (пользу) rhAPC (см. приложение B для абсолютных противопоказаний). Воспалительный ответ при тяжелом сепсисе интегрально связан с прокоагулянтной активностью и эндотелиальной активизацией. Воспалительный ответ при сепсисе является прокоагулянтным на ранних стадиях. RhAPC, эндогенное противосвертывающее средство с противовоспалительными свойствами, показал в большом, мультицентровом, рандомизированном, контролированном испытании улучшение выживания у пациентов с сепсис – индуцированной органной дисфункцией.
Введение препаратов крови. Как только гипоперфузия тканей устранена и при отсутствии отягощающих обстоятельств, типа существенной болезни коронарной артерии, острого кровоизлияния или молочно-кислого ацидоза (см. рекомендации по начальному восстановлению), переливание эритроцитов должно быть выполнено только тогда, когда гемоглобин уменьшен до ‹ 7.0 g/dl (‹ 70 g/1), добиваясь увеличения гемоглобина до 7.0–9.0 g/dl (70–90 g/1). Хотя оптимальный гемоглобин для пациентов с тяжелым сепсисом не был специально исследован, требования к Переливаниям в Критической Медицине (Transfusion Requirements in Critical Care – TRICC) диктуют гемоглобин 7–9 г/дл (70–90 г/л), по-скольку он адекватен для большинства критических пациентов. Трансфузионный порог 7.0 g/dl (70 g/1. не был связан с увеличением смертности. Переливание эритроцитов у септических пациентов увеличивает доставку кислорода, но обычно не увеличивает его потребление [51, 52, 53]. Этот трансфузионный порог контрастирует с целевым гематокритом 30 % у пациентов с низким центральным венозным O2 – насыщением в течение первых 6 часов восстановления при септическом шоке.
Эритропоэтин (Erythropoietin) не рекомендуется, как определенное лечение анемии, связанной с тяжелым сепсисом, но может использоваться, когда септические пациенты имеют другие объективные причины для введения эритропоэтина, типа почечной недостаточности индуцирующей (вызывающей) компрометацию продукции эритроцитов.
Место иммунотерапии сепсиса
Разработка новых агентов для терапии сепсиса основывается на положении, что нейтрализация бактериальных токсинов или потенциально повреждающих медиаторов иммунной системы может излечить септический процесс или, по крайней мере, замедлить его. Эти новые терапевтические стратегии направлены против различных элементов гипервоспалительного каскада, к которому относятся бактериальные токсины, такие как эндотоксин или следующие за ним медиаторы (ФНО и ИЛ-1). Для этого в экспериментах на животных и в клинических исследованиях использовали в качестве терапевтических средств моноклональные или поликлональные антитела против токсинов, моноклональные антитела против медиаторов, антагонисты медиаторов или иммуноглобулины. В Европе и СНГ (1998 г.) для клинического испытания был допущен моноклональный специфический антилипид А- IgM, антитела HA-IA. Полученные негативные данные заставили изъять препараты из употребления. Несмотря на разочаровывающие результаты, это не значит, что эндотоксин не является подходящей целью для терапии сепсиса. Тем не менее, остается недоказанной гипотеза, что антитела против ядра эндотоксина являются защитными.
Терапия иммуноглобулинами
С начала нынешнего столетия для профилактики и терапии различных инфекционных болезней успешно применяют различные иммуноглобулиновые препараты.
Постулируется, что в/в иммуноглобулины эффективны, благодаря связыванию и нейтрализации микробных антигенов, нейтрализации токсинов, благодаря блокаде связывания вирусов и бактерий с целевой клеткой и в результате их активности как опсонинов, инициирующих схватывание и деградацию патогенов фагоцитирующими клетками. Иммуноглобулиновые препараты содержат также нейтрализующие антитела против суперантигенов, таких как стафилококковые токсины, которые, как полагают, играют важную роль при дисрегуляции иммунитета.
Важным для клинической практики представляется тот факт, что при тяжелых инфекциях уровень всех иммуноглобулинов, в том числе и IgM, может быть сильно снижен.
Пациенты с низкими титрами антител более часто демонстрируют эпизоды с лихорадкой и повышенную летальность грамотрицательного и эндотоксинположительного септического шока.
Терапия пентаглобином, благодаря повышенной концентрации IgM- и IgG-антител против ядра эндотоксина, обеспечивает высокое защитное действие. Так как пентаглобин получают из пула человеческой плазмы, он содержит также большие количества антител против иммунодоминантных видоспецифических боковых цепочек эндотоксина, которые должны защищать от гомологичных бактерий. Из всех имеющихся иммуноглобулинов доказанной считается только эффективность пентаглобина.
Многие пациенты с сепсисом иммунокомпетентны. Они хорошо реагируют на стандартные антибиотики и кардиоваскулярную поддержку. Они дают адекватную воспалительную реакцию, которая контролирует инфекцию и элиминирует бактериальные токсины (табл. 4). Неадекватный воспалительный ответ на инфекцию может развиться у других пациентов с подавленными в результате терапии стероидами, с нейтропенией, политравмами иммунитета, генетическим или приобретенным иммунодефицитом. У этих пациентов усиление защитных механизмов может поддержать клиренс бактерий и их токсинов и снизить повреждение тканей.
Длительный опыт применения внутривенных иммуноглобулинов класса IgM и IgG позволяет оценить эффективность препаратов. Показания и дозировки претерпели за эти годы изменения. Пассивная иммунизация наряду с активной прочно заняла свое место. Является неоспоримым, что применение иммуноглобулинов при правильном показании, достаточной дозировке и в верно выбранный момент времени может спасти жизнь пациента.
Однако антитоксическая и антивоспалительная иммунная терапия сепсиса оказалась труднее, чем думали вначале. Причина этого заключается, наверняка, в том, что мы пока находимся «в эмбриональной фазе патофизиологического понимания сепсиса». Кроме того, клинический опыт показывает, что при сепсисе далеко не всегда имеются нарушения гуморального звена иммунитета, а изменения иммунного гомеостаза носят гораздо более сложный характер. По-этому применение заместительной иммунотерапии даже пентоглобином не может принципиально повлиять на результаты лечения сепсиса.
Наш опыт лечения сепсиса
Мы располагаем опытом лечения свыше 2000 больных сепсисом, причем, основная масса (больше 60%) больных поступала в тяжелом состоянии (20–25 баллов и выше по шкале APACHE II).
В основу лечения положена традиционная санация возможных очагов инфекции и антибактериальная терапия.
Особое внимание уделяется ранней диагностике и санации возможных очагов инфекции, сепсиса, т.к. при невыполнении этого первого и главнейшего требования эффект от лечения будет отсутствовать. Локализация этих очагов может быть самой различной: хронические инфекции ротоглотки, дыхательных путей, абсцессы брюшной полости, постинъекционные абсцессы, дисбиоз кишечника, инфекции мочеполового тракта, внутривенные и уретральные катетеры, повязки, тампоны и т. д.
Антибактериальную терапию условно разделяют на эмпирическую (предположительную) и точную.
Эмпирическая терапия
Эмпирическая терапия предусматривает введение антибиотиков при явных признаках инфекции еще до идентификации возбудителя. Она основана на чувствительности вероятного возбудителя, вызвавшего инфекционный процесс. Ценную информацию дает бактериоскопическое исследование биологического материала, получаемого из инфекционных очагов при их санации с обязательной окраской по Грамму. Результаты данного исследования можно получить уже через 30 минут после забора материала и на их основе назначить эмпирическую терапию. В качестве эмпирической терапии, как правило, назначаются антибиотики широкого спектра действия.
Точная терапия
Точная терапия направлена на один или более микроорганизм, чья роль у пациентов определена (выделение возбудителя из крови и подтверждение с помощью реакции агглютинации с выделенным возбудителем). Выбирается наиболее специфичный и наименее токсичный препарат. Положительные результаты посевов из крови получались нами примерно в 30 % случаев, что соответствует данным, имеющимся в литературе.
Однако в последние годы отмечено резкое снижение частоты положительных результатов посевов (20,1%), что объясняется, воз-можно, мощной антибактериальной терапией, которая проводилась больным до поступления в наш стационар. В связи с этим, нами про-водится тщательный анализ результатов посевов на гемокультуру у больных, поступивших в противосептический центр. Посевы выполняются в первые сутки пребывания больных в стационаре. Выделение и идентификация микроорганизмов проводится системой Bactek-Phoenix. Начало точной терапии было возможным не ранее чем через 72 часа. Еще 5–7 лет назад преобладала Грам+ флора (73,6 %), чувствительность которой к тиенаму составила 98,8 %, к цефалотину – 96 %, к нетромицину – 79,7 %. грамм – флора составила 26,4 %, причем, она была чувствительной практически только к тиенаму. Из 209 посевов крови в течение 2006 года положительный результат получен в 42 случаях, что составляет 20,1%. Ведущими в качестве микробного этиологического фактора сепсиса служат грампозитивные микроорганизмы (59%), такие как представители рода Staphylococcus: St. aureus, St. haemolyticus, St. hominis, St. Epidermidis. Процент грамне- гативных организмов составил 31% и они были представлены семейством Enterobacteriaceae, родов Es^en^ia (E. Coli), Proteus, Morganella, а так же Pseudomonas aeruginosa На грамположительные микроорганизмы, представленные родом Staphylococcus, действовали ванкомицин, линезолид и рифампицин в 100%, в 60% – макролиды. На грамотрицательные бактерии наиболее эффективно воздействовали карбопенемы, новейшие аминогликозиды, фторхинолоны, монобактамы, III поколение цефалоспоринов и защищенные пенициллины. Полученные данные позволяют оптимизировать антибиотикотерапию.
Еще одним немаловажным моментом является то, что эндотоксин выделяется при гибели микроорганизмов под действием антибиотиков. Причем, степень выделения эндотоксина неодинакова. Токсинообразование увеличивается в следующем порядке: тиенам – аминогликозиды – фторхинолоны – цефалоспорины (более всего). Исходя из этого, при назначении антибиотика септическому больному следует учитывать степень имеющегося у него эндотоксикоза, а также возможное его усугубление в результате действия данного препарата.
В основном мы придерживались эмпирической антибактериальной терапии, применяя антибиотики широкого спектра действия с учетом их влияния на токсинообразование.
Детоксикационная терапия
У тяжелых больных с выраженной эндотоксемией считаем обязательным применение методов экстракорпоральной детоксикации (плазмаферез, гемоперфузия, гемодиафильтрация). Выбор метода и частота применения экстракорпоральной детоксикации зависели от тяжести состояния и характера развития полиорганной дисфункции. Наиболее продуктивным способом прерывания цитокинового каскада является плазмаферез. В нашей клинике проводится непрерывный плазмаферез с использованием аппарата фирмы «Фрезениус» или плазмофильтрация с помощью плазмофильтров этой же фирмы. При выраженной ферментемии и протеолизе (перитонит, панкреатит и др.) методом выбора становится многократная перфузия крови через «Овосорб». Полиорганная дисфункция с нарушением функции почек требует применения гемодиафильтрации с использованием мембран повышенной проницаемости. Экстракорпоральная детоксикация практически всегда приводила к улучшению общего состояния больных и существенно влияла на исход заболевания. Раннее применение экстракорпоральной детоксикации существенно усиливает медикаментозную терапию и, прежде всего, антибактериальную терапию, так как меняет степень блокирования всех систем жизнеобеспечения токсинами.
Применение ингибиторов TNF и нестероидных противовоспалительных препаратов, по нашему мнению, не влияло на течение сепсиса и исход.
Иммунотерапия
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
50. Патогенез сепсиса
50. Патогенез сепсиса Микроорганизмы по-прежнему считаются главной причиной возникновения сепсиса, определяющей его течение, причем решающее значение имеют вирулентность возбудителя, его доза (титр микроорганизмов должен быть не менее 10: 5 в грамме ткани). Крайне важными
52. Септические осложнения. Лечение сепсиса
52. Септические осложнения. Лечение сепсиса Инфекционно-токсический шок имеет сложный патогенез: с одной стороны, бактериальные токсины вызывают снижение тонуса артериол и нарушение в системе микроциркуляции, с другой – наблюдается нарушение системной гемодинамики в
2. Патогенез сепсиса
2. Патогенез сепсиса Микроорганизмы по-прежнему считаются главной причиной возникновения сепсиса, определяющей его течение, причем решающее значение имеют вирулентность возбудителя, его доза (титр микроорганизмов должен быть не менее 10 : 5 в грамме ткани). Крайне важными
4. Септические осложнения. Лечение сепсиса
4. Септические осложнения. Лечение сепсиса Основными осложнениями сепсиса, от которых и погибают больные, следует считать:1) инфекционно-токсический шок;2) полиорганную недостаточность.Инфекционно-токсический шок имеет сложный патогенез: с одной стороны, бактериальные
Теодор Бильрот (Австрия, 1829–1894) Грязь в госпиталях — причина сепсиса*
Теодор Бильрот (Австрия, 1829–1894) Грязь в госпиталях — причина сепсиса* Еще в середине прошлого столетия среди хирургов господствовало убеждение, что жизнь человека на операционном столе подвергается большей опасности, чем на поле брани. В хирургических отделениях многих
8.4. ИНТЕНСИВНАЯ РЕАБИЛИТАЦИЯ ПРИ ВЫРАЖЕННЫХ ДИСПЛАСТИЧЕСКИХ ПРОЯВЛЕНИЯХ В ОПОРНО-ДВИГАТЕЛЬНОМ АППАРАТЕ
8.4. ИНТЕНСИВНАЯ РЕАБИЛИТАЦИЯ ПРИ ВЫРАЖЕННЫХ ДИСПЛАСТИЧЕСКИХ ПРОЯВЛЕНИЯХ В ОПОРНО-ДВИГАТЕЛЬНОМ АППАРАТЕ П. 1. Тракционная ротационная манипуляционная технология в течение недели.П. 2. Продолжая способ, указанный в П.1, со 2-й недели на фоне купирования спастических
Интенсивная инсулинотерапия. Введение инсулина при утренней гипогликемии
Интенсивная инсулинотерапия. Введение инсулина при утренней гипогликемии Интенсивная инсулинотерапия применяется с целью достичь компенсации диабета на длительное время и добиться профилактики поздних сосудистых осложнений диабета.Существуют определенные правила
Глава 8 Интенсивная неврологическая терапия
Глава 8
Интенсивная программа упражнений
Интенсивная программа упражнений Выполняя подготовительные упражнения, вы научились самому главному: тому, как правильно держать голову и как активировать слаборазвитые рудиментарные ушные мышцы. Этого достаточно, чтобы начать целенаправленную тренировку
II. Мануальная терапия внутренних органов, или Старославянская терапия живота
II. Мануальная терапия внутренних органов, или Старославянская терапия живота «Бог помогает тому больше, кто помогает себе чаще». Английская пословица Мануальная терапия живота До настоящего времени ученые считали, что у человека есть два мозга — головной и спинной.
Интенсивная инсулинотерапия
Интенсивная инсулинотерапия Интенсивная инсулинотерапия применяется с целью достичь компенсации диабета на длительное время и добиться профилактики поздних сосудистых осложнений диабета.Существуют определенные правила проведения инсулинотерапии. Так, перед каждой
Паршвоттанасана — Интенсивная боковая растяжка
Паршвоттанасана — Интенсивная боковая растяжка parsva — бок, сторона; ut — сильный, интенсивный; tan — тянуть, растягивать Классификация и уровень сложностиБазовая асимметричная стойка в наклоне.Движения костей и суставовНезначительное сгибание позвоночника.Нога,
Интенсивная технология выращивания шиитаке
Интенсивная технология выращивания шиитаке В первую очередь для производства грибов шиитаке необходимо создать питательный субстрат, подбирая для этого компоненты хорошего качества. Стружка и опилки деревьев лиственных пород, используемые в субстрате, должны быть
3. Интенсивная ходьба
3. Интенсивная ходьба После 3 – 5-минутной разминки вы перейдете на очень быстрый темп (позиция 7–8 шкалы ИВН) на все время тренировки, которую, как обычно, закончите 3–5 минутами
Интенсивная аэробика: загоняем добычу
Интенсивная аэробика: загоняем добычу Интенсивные упражнения, заставляющие ваш сердечный ритм подниматься выше 65 % от максимума, требуют перехода на другое топливо. Жир уже не может обеспечить всю необходимую энергию, так что мускулатура начинает сжигать глюкозу. Меняя