11. Является ли официальная медицина злом?
11. Является ли официальная медицина злом?
Итак, это была индустрия альтернативной медицины. Ее заявления адресованы непосредственно публике, поэтому они распространены гораздо больше; и в то время как ее торговые уловки почти те же, что и у фармацевтической промышленности — мы имели возможность в этом убедиться, — ее стратегии и ошибки более очевидны и поэтому представляют собой прекрасное учебное пособие. Ну что ж, нам следует постараться изменить игру.
В этой главе вам также придется подняться над вашим самолюбованием. Мы не будем говорить о том, что ваш участковый врач иногда спешит, или о том, что врачи иногда грубы. Мы не будем говорить о том, что никто не мог понять, что было с вашим коленом, даже не будем обсуждать, что когда-то вашему дедушке не смогли вовремя диагностировать рак и он зря страдал несколько месяцев перед болезненной, кровавой, незаслуженной и недостойной смертью в конце своей продуктивной и счастливой жизни.
В медицине случаются ужасные вещи, и когда она все делает правильно, и когда она ошибается. Все согласны с тем, что количество ошибок должно быть минимальным, все согласны, что врачи иногда бывают ужасны; если этот предмет вас интересует, я советую вам купить одну из книг по вопросам клинической политики, достойную находиться в библиотеке. Врачи могут быть ужасными, ошибки могут быть смертельными, но философия, управляющая доказательной медициной, — нет. Насколько хорошо она работает?
Вы можете попробовать определить, насколько медицинская практика основана на доказательствах. Это нелегко. Исходя из современных данных, около 13 % всех видов лечения имеют веские доказательства пользы и еще 21 %, вероятно, являются полезными.
Это низкие цифры, но, по-видимому, наиболее распространенные методы имеют лучшую доказательную базу. Еще один способ измерить это — посмотреть на то, какая часть медицинской деятельности является доказательной: взять последовательно несколько пациентов в поликлинике, посмотреть их диагнозы и лечение, которое они получали, а затем выяснить, был ли выбор лечения основан на доказательствах. Эти исследования из реального мира дают более значимые цифры: множество таких исследований было проведено в 1990-е годы, и оказалось, что в зависимости от специальности от 50 до 80 % всей медицинской деятельности является доказательной. Не так уж много, и если у вас есть идеи, как это улучшить, пожалуйста, напишите об этом[37].
Еще один способ — посмотреть, что случится, если что-то пойдет не так. «Британский медицинский журнал», вероятно, является самым авторитетным медицинским журналом в стране. Недавно он назвал три самые популярные статьи из его архива за 2005 год, определенные на основании данных проверки, которая оценивала интерес к ним читателей, количество ссылок на них в других научных статьях и т. д. Каждая из этих статей содержала критику либо лекарства, либо фармацевтической фирмы, либо медицинской деятельности (это была центральная тема всех трех статей).
Мы можем кратко пройтись по их содержанию, чтобы вы могли оценить, насколько самые читаемые статьи из крупнейшего медицинского журнала соответствуют вашим потребностям. Самая популярная статья была посвящена испытаниям «случай-контроль», которые показали, что пациенты имели более высокий риск сердечного приступа, если принимали лекарства рофекоксиб (Vioxx), диклофенак или ибупрофен. В статье номер два был большой метаанализ данных фармацевтической компании, который не подтвердил, что антидепрессанты СИОЗС (селективные ингибиторы обратного захвата серотонина) повышают риск самоубийства, но зато показал, что эти лекарства увеличивают риск намеренного причинения себе вреда. На третьем месте был систематический обзор, который показал связь между попытками самоубийства и использованием СИОСЗ и критически осветил некоторые несоответствия вокруг сообщений о самоубийствах в клинических испытаниях.
Это критический подход и это правильно, но вы можете заметить кое-что еще: все эти исследования вращались вокруг ситуаций, где фармацевтические фирмы утаили или исказили данные. Как это происходит?
Фармацевтическая индустрия
Торговые уловки, которые мы обсудим в этой главе, вероятно, более сложные, чем все остальное, о чем говорится в этой книге, поскольку мы собираемся представить техническую критику профессиональной литературы в этой области. К счастью, фармацевтические компании не адресуют свою рекламу непосредственно широкой публике в Великобритании (в США вы можете найти рекламу таблеток, снимающих беспокойство у собак), поэтому мы будем критиковать те уловки, которые они используют для врачей, аудитории, которая лучше может распознать их блеф. Это означает, что мы сначала должны объяснить, как лекарство попадает на рынок. Это то, чему будут учить в школе, когда я стану президентом единого мирового правительства.
Понимание этого процесса важно по одной явной причине. Мне кажется, что многие странные идеи, которые возникают у людей, имеют корни в эмоциональной борьбе с самим понятием «фармацевтическая промышленность». Каковы бы ни были наши политические взгляды, мы все становимся социалистами, когда речь идет о здравоохранении. Мы все нервничаем, когда думаем о том, что прибыль может играть роль в профессии врача, но это ощущение никуда не пришьешь. Крупные фармацевтические фирмы — это зло: я готов согласиться с этой предпосылкой. Но поскольку люди не понимают толком, как они причиняют зло, их гнев и возмущение существуют отдельно от здравой критики, которую фармацевтические фирмы заслужили за то, что искажают данные испытаний, или, например, отказываются поставлять спасительные лекарства от СПИДа в развивающиеся страны. Обывательская критика больше похожа на детские фантазии. «Крупные фармацевтические фирмы — это зло, — рассуждают обыватели, — поэтому гомеопатия работает, а вакцина против MMR приводит к аутизму». Это тупиковый путь.
В Великобритании фармацевтическая промышленность стала третьей по прибыльности после финансового сектора и — вы удивитесь, если вы британец — туризма. Мы тратим семь миллиардов фунтов в год на лекарства, и из них 80 % уходит на патентованные средства, препараты, которые были выпущены за последние десять лет. В целом эта отрасль стоит 150 миллиардов фунтов.
Фармацевтические корпорации должны увеличивать свою прибыль, и это не всегда согласуется с идеей заботы о людях. Крайний пример — это пример со СПИДом: я мимоходом о нем упоминал, фармацевтические компании объясняли, почему они не могут продавать лекарства по низкой цене в развивающиеся страны. Им требуются деньги на исследования и новые разработки. Однако из прибыли в 200 миллиардов долларов, которую получают крупнейшие американские компании, они тратят на исследования только 14 % по сравнению с 31 % на маркетинговые нужды.
Они также устанавливают на свою продукцию цены, которые можно назвать грабительскими. Если лекарство выходит на рынок, у вас есть десять лет на патент, то есть исключительное право его производить. Лоратадин, выпускаемый компанией «Шеринг-Плау», представляет собой эффективный антигистаминный препарат, который не вызывает неприятного побочного эффекта в виде сонливости. В течение какого-то времени оно было единственным и очень популярным. До истечения срока патента цена на лекарство поднималась 13 раз за пять лет и выросла на 50 %. Некоторые могут подумать, что это выгодно.
Но фармацевтическая промышленность постоянно испытывает проблемы. Золотой век медицины подошел к концу, как мы уже сказали, и количество новых лекарств, или «новых молекулярных категорий», снизилось с 50 в год в 1990-е годы примерно до 20 в год сейчас. В то же время выросло количество аналогов, которые составляют до половины новых наименований.
Лекарства-аналоги, или дженерики, — это неизбежная реальность рынка: примерные копии лекарств, которые уже существуют, произведенные другой компанией, но достаточно отличающиеся от них, чтобы претендовать на новый патент. Они производятся с большими усилиями и нуждаются в испытаниях (на людях, со всеми сопутствующими рисками), чтобы затем быть выпущенными на рынок как новые препараты. Иногда они имеют небольшое преимущество (более удобная дозировка, например), но если учесть всю огромную работу, которая требуется для их выпуска, они как-то не выглядят значительным прорывом в медицине. Это прорыв в получении прибыли. Откуда же все они берутся?
Путешествие лекарства
Прежде всего, нужна идея лекарства. Она может прийти откуда угодно: молекула в растении; рецептор в организме, к которому вы можете подобрать нужную молекулу; старое лекарство, которое вы собираетесь усовершенствовать, и т. д. Эта часть истории очень интересна, рекомендую защитить по ней диссертацию. Когда вы думаете, что «поймали» молекулу, которая может пригодиться, вы тестируете ее на животных, чтобы посмотреть, работает ли она так, как вы предполагали (и в то же время, конечно, посмотреть, не убивает ли она их).
Затем наступает фаза 1, или «первая на людях», исследования на небольшой группе смелых, здоровых молодых людей, которым нужны деньги, во-первых, чтобы посмотреть, не убьет ли их это лекарство, а также чтобы измерить некоторые важные вещи, например, как быстро оно выводится из организма (это та фаза, которую не прошел иммуномодулятор TGN-1412 в 2006 году, когда несколько молодых людей серьезно пострадали во время испытаний). Если лекарство работает, вы выходите на фазу 2, то есть проводите испытания на двух сотнях людей, имеющих ту самую болезнь, для лечения которой предназначен препарат. Эта фаза должна «доказать концепцию», определить дозу и дать представление об эффективности. Здесь терпят неудачу многие препараты, и это позор, поскольку это не школьный проект: выпустить лекарство на рынок стоит 500 миллионов долларов.
Затем вы переходите к фазе 3, испытаниям лекарства на сотнях и тысячах пациентов, рандомизированным и слепым, сравниваете ваш препарат с плацебо или с другим лекарством и собираете больше данных о его эффективности и безопасности. Вам может потребоваться несколько таких испытаний, а затем вы можете обратиться за получением лицензии на его продажу. После появления лекарства на рынке вы должны проводить дополнительные клинические испытания и другие исследования вашего препарата; возможно, кто-то обратит внимание на его побочные эффекты, которые не были замечены ранее, в идеале используя систему «желтой карты» (ее могут использовать и пациенты). Подробнее об этом см.: http://medi.ru/doc/9920io2.htm.
Врачи принимают собственное решение по поводу того, хотят ли они прописывать лекарство на основании данных о его эффективности в клинических испытаниях, отмеченных побочных эффектах и иногда стоимости. В идеале они получают эту информацию из статей, опубликованных в солидных академических журналах, или из материалов типа учебников или обзорных статей, которые сами базируются на первичных исследованиях лекарств. В худшем случае они полагаются на ложь представителей фармкомпаний или слухи.
Испытания лекарств стоят дорого, поэтому до 90 % клинических испытаний и 70 % испытаний, о которых написано в основных медицинских журналах, проводятся или финансируются фармацевтической индустрией. Ключевая черта научного исследования — это то, что его результаты должны быть воспроизводимыми, но если только одна организация обеспечивает финансирование, эта черта отсутствует.
Возникает искушение обвинить фармацевтические фирмы — хотя мне кажется, что государственные и общественные организации несут равную ответственность за то, что не вмешиваются — но где бы вы ни проводили свою нравственную линию, результат один: компании, производящие лекарства, оказывают огромное влияние на то, что именно исследуется, как исследуется, как преподносятся результаты, как они анализируются и как интерпретируются.
Иногда из-за недостатка средств и интереса со стороны корпораций целые области оказываются без внимания. Гомеопаты и шарлатаны с витаминными пилюлями расскажут вам, что их продукция — это хороший пример такого явления. Однако это нравственный вызов другим примерам. Есть болезни, которые поражают небольшое число людей, такие как болезнь Крейцфельда — Якоба или болезнь Вильсона, а еще более страшно то, что есть болезни, которыми пренебрегают, поскольку они встречаются только в развивающихся странах, такие как болезнь Шагаса (которая угрожает четверти латиноамериканского населения) и трипаносомоз (300 000 случаев в год, но в Африке). Глобальный форум по исследованиям в области здравоохранения подсчитал, что 90 % финансирования на биомедицинские исследования получают лишь 10 % мировых медицинских проблем.
Часто не хватает только информации, а не удивительной новой молекулы. Эклампсия, скажем, по оценкам, ежегодно вызывает 50 000 смертей среди беременных женщин во всем мире, и лучшее лечение — это дешевый, непатентованный сульфат магния (высокие дозы внутривенно). Это не альтернативные медицинские добавки, но также недорогое противосудорожное средство, которое использовалось многие годы. Хотя сульфат магния использовался для лечения эклампсии с 1906 года, его позиция как лучшего метода при этом заболевании получила официальное подтверждение только в 2002 году с помощью ВОЗ, поскольку к исследованиям в этой области не было коммерческого интереса — ни у кого не было патента на магний, а большинство смертей от эклампсии происходит в развивающихся странах. С 1906 года от эклампсии умерли миллионы женщин, и очень многих смертей можно было бы избежать.
В какой-то степени это проблемы политические и экономические, и их мы пока оставим; мне нужно выполнить данное вам обещание: вы хотите понять с помощью того, что вы уже знаете о научных доказательствах и исследованиях, как фармацевтические компании искажают данные и надевают шоры на ваши глаза. Как это доказать? В целом верно, что испытания, проводимые фармацевтической компанией, с большей вероятностью дают положительные результаты, если дело касается ее собственного лекарства. Но ограничиться только этим утверждением было бы недальновидно.
Этот пример я привожу студентам-медикам и врачам в лекции, которую читаю время от времени, и привык называть «фармацевтическое дерьмо». Меня, в свою очередь, научили этому в медицинской школе, и я думаю, что самый легкий способ понять это — влезть в шкуру исследователя фармацевтической компании.
У вас есть пилюля. Она хорошая, может, не блестящая, но она может принести кучу денег. Вам нужен положительный результат, но ваша аудитория — это не гомеопаты, не журналисты и не широкая публика. Эго врачи и ученые, поэтому они видят все ваши очевидные уловки типа «испытаний не Вслепую» или «неадекватной рандомизации». Ваши манипуляции должны быть более тонкими, более элегантными, но более эффективными.
Что вы можете сделать?
Во-первых, вы можете изучать лекарства на «победителях». Разные люди по-разному реагируют на лекарства: старики для большинства лекарств безнадежны, в то время как молодые люди с единственным заболеванием гораздо более перспективны. Поэтому испытывайте свое лекарство на молодых. Это сделает его менее эффективным для реальных больных, которым его будут прописывать, но, может, они не заметят. Подобная позиция исследователей настолько часто встречается, что не стоит и приводить примеры.
Далее, вы можете сравнивать свое лекарство с бесполезным контрольным. Многие люди скажут, что вы не должны сравнивать лекарство с плацебо, потому что это не доказывает его клинической ценности. В реальном мире никого не интересует, лучше ли ваше лекарство, чем сахарная пилюля; их больше интересует, лучше ли оно, чем существующее лечение. Но вы уже потратили несколько миллионов долларов на то, чтобы произвести это лекарство, поэтому нужно делать следующее: множество испытаний с плацебо-группой и побольше шума по этому поводу, поскольку положительный результат практически гарантирован. И снова это применяется повсеместно, так как все лекарства можно сравнивать с плацебо на какой-то стадии, и люди, нанятые фармкомпаниями, чтобы дурить врачей (многие просто отказываются их посещать), с удовольствием сообщат о бесспорном успехе этих испытаний.
Дальше все становится интереснее. Если вы хотите сравнить ваше лекарство с другим, производимым фирмой-конкурентом, — чтобы сохранить лицо или потому что так требуют контролирующие организации, — можете попробовать хитрый трюк: используйте неадекватную дозу конкурирующего лекарства, так что пациенты, принимающие его, не будут чувствовать себя очень хорошо, или дайте слишком большую дозу конкурирующего лекарства, и у пациентов будет больше побочных эффектов, или давайте конкурирующее лекарство недолжным образом (перорально, когда оно обычно дается внутривенно — может, опять- таки не заметят), или увеличивайте дозу конкурента слишком быстро, тогда побочные эффекты будут сильнее. На этом фоне ваше лекарство засияет.
Вы можете подумать, что такие вещи в реальности не происходят. Если вы посмотрите примечания в конце книги, вы найдете исследования, где пациентам давали слишком высокие дозы устаревшего антипсихотического препарата (что дало возможность лекарствам нового поколения выглядеть лучше в смысле побочных эффектов), или исследования дозировки антидепрессантов СИОЗС, которые некоторым могли показаться необычными, — это только два примера. Я знаю, что это звучит слегка неправдоподобно.
Конечно, еще один трюк с побочными эффектами — это просто не спрашивать о них или, — поскольку вам приходится изворачиваться, — спрашивать осторожно. Вот вам пример. Антидепрессанты СИОЗС довольно часто вызывают побочные эффекты в сексуальной сфере, включая аноргазмию. Следует внести абсолютную ясность (я постараюсь сформулировать это как можно нейтральнее): мне нравится ощущение оргазма. Оно для меня важно, и весь мой опыт подсказывает, что это ощущение важно и для других людей. Ради этого ведутся настоящие войны. Некоторые психологи-эволюционисты даже будут пытаться убедить вас, что вся человеческая культура и язык управляются в значительной степени стремлением к достижению оргазма. Утрата этого ощущения кажется важным побочным эффектом, о котором стоит спрашивать.
Однако различные исследования показали, что сообщенная частота аноргазмии у пациентов, принимающих СИОЗС, варьирует от 2 до 73 %, в зависимости от того, как вы спрашиваете: случайный, заданный мимоходом вопрос о побочных эффектах или тщательный, подробный опрос. В одном исследовании СИОЗС, включавшем 3000 пациентов, побочные эффекты в сексуальной сфере даже не были включены в таблицу побочных эффектов из 23 пунктов. Двадцать три другие вещи были более важными, по мнению исследователей, чем потеря ощущения оргазма. Я прочитал этот список. По-моему, нет.
Но вернемся к основным результатам. Вот еще один трюк: вместо реальных результатов, таких как смерть или боль, вы можете использовать суррогатные, которые получить гораздо легче. Если ваше лекарство должно снижать уровень холестерина в крови и предотвращать смерть от сердечных приступов, не отмечайте случаи смерти от сердечных приступов, измеряйте только уровень холестерина: снижения его достигнуть гораздо легче, чем снижения смертности от сердечных болезней, а испытание будет дешевле и быстрее, и результат, соответственно, будет дешевле и положительнее. Результат!
Допустим, что вы провели свое испытание, и, несмотря на все ваши усилия, результат отрицательный. Что можно сделать? Если ваши испытания были хорошо проведены, но дали некоторые отрицательные результаты, можете попробовать старый фокус: не привлекайте внимание к разочаровывающим данным, рисуя графики. Упомяните об этом кратко в тексте и проигнорируйте, когда будете делать выводы. (Мне самому это отлично удается. Это результат того, что я много читаю о подобных испытаниях.)
Если ваши результаты целиком отрицательные, не публикуйте их совсем или публикуйте много времени спустя. Это именно то, что было сделано с результатами испытаний СИОЗС: они скрыли данные, предполагая, что это может быть опасно, и умолчали о том, что эти лекарства действуют не лучше, чем плацебо. Если вы действительно умный и у вас есть деньги, которых вам не жалко, то после получения разочаровывающих данных вы можете провести еще испытания с тем же протоколом, в надежде, что результаты будут положительными, затем попытаться свести данные вместе, так что ваши отрицательные результаты будут поглощены какими-нибудь посредственными положительными.
Или вы можете стать серьезным или начать манипулировать статистикой. Только на следующие две страницы эта книга станет несколько занудной. Я пойму, если вы захотите пропустить их.
Но знайте, что эта информация здесь для врачей, которые купили эту книгу, чтобы посмеяться над гомеопатами. Вот вам классические трюки со статистическим анализом, чтобы обеспечить положительные результаты ваших испытаний.
Полностью игнорируйте протокол
Всегда допускайте, что любая зависимость доказывает причинную связь. Внесите все ваши данные в программу и сообщайте — как о чем-то важном — о любой взаимосвязи между всем чем угодно, если это работает на вас. Если вы измерите все, то что-то, несомненно, окажется положительным, просто благодаря случаю.
Манипулируйте с линией отсчета
Иногда, когда вы начинаете испытания, группа, получающая лечение, уже чувствует себя лучше, чем группа плацебо. Если это так, то оставьте все как есть. Если, с другой стороны, плацебо- группа чувствует себя лучше в начале испытаний, подправьте линию отсчета в вашем анализе.
Игнорируйте выбывших
Люди, которые выбывают из испытаний, с точки зрения статистики, скорее всего, чувствуют себя хуже, и у них, вероятно, наблюдаются побочные эффекты. Они только испортят имидж вашего лекарства. Поэтому игнорируйте их, не пытайтесь их вернуть и не включайте в ваш окончательный анализ.
Подчистите данные
Посмотрите на ваши графики. Там наверняка найдутся аномалии, или точки, которые располагаются далеко от остальных. Если они не в вашу пользу, исключите их. Если они помогают поддержать имидж вашего лекарства, оставьте их на месте, даже если это выглядит неправдоподобно.
Пять… нет, семь… нет, девять!
Если разница между вашим лекарством и плацебо становится значительной через четыре с половиной месяца, а испытание запланировано на шесть, прекратите испытание досрочно и зафиксируйте результаты: они могут стать менее впечатляющими, если вы продолжите. И наоборот, если через шесть месяцев результаты будут «почти положительными», продолжите испытания еще на три месяца.
«Помучайте» данные
Если результаты совсем плохи, попробуйте вернуться назад и посмотреть: может быть, в какой-нибудь подгруппе они другие. Вдруг вы обнаружите, что лекарство хорошо работает на китайских женщинах в возрасте от 52 до 61 года? «Помучайте данные, и они во всем сознаются», — как говорят в тюрьме Гуантанамо.
Понажимайте все кнопки на компьютере
Если вы в отчаянии, и анализ данных тем способом, который вы планировали, не дает нужных вам результатов, попробуйте другие статистические анализы, даже если они сюда совершенно не подходят, просто наугад.
И когда вы закончили, самое главное — это напечатать ваши результаты с умом. Если испытания удались, смело печатайтесь в самом крупном журнале, какой только сможете найти. Если результаты положительные, но вы слегка слукавили и это может выйти наружу, тогда печатайте их в малоизвестном журнале (который пишется и издается исключительно промышленностью): помните, что все уловки, которые мы только что описали, ничего не скрывают, и станут явными для любого, кто прочитает вашу статью, но только при внимательном чтении, поэтому в ваших интересах, чтобы никто не читал дальше введения. И наконец, если ваши результаты действительно смущают, спрячьте их подальше и ссылайтесь на них как на «данные в файле». Никто не будет знать ваши методы, и их заметят, только если кто-нибудь начнет их искать для систематического обзора. Остается надеяться, что это произойдет нескоро.
Как это возможно?
Когда я объясняю эти манипуляции с результатами своим друзьям, которые не являются медиками или учеными, они очень удивляются. «Как же это возможно?» — спрашивают они. Во-первых, многие плохие исследования объясняются некомпетентностью. Но многие методологические ошибки, описанные выше, представляют собой намеренный обман. Можно ли разоблачить грязную игру?
На индивидуальном уровне иногда чрезвычайно трудно доказать, что испытание было намеренно подделано, чтобы продемонстрировать результаты, нужные спонсорам. Но в целом картина вырисовывается довольно ясно. Этот вопрос так часто изучался, что в 2003 году один систематический обзор обнаружил 30 исследований, целью которых было посмотреть, влияет ли финансирование в разных группах испытаний на их результаты. Исследования, финансируемые фармацевтическими компаниями, как было показано, в четыре раза чаще независимых давали результаты, благоприятные для компаний.
Один обзор тенденциозных исследований рассказывает историю, поистине достойную «Алисы в стране чудес». Было найдено 56 различных испытаний, сравнивающих обезболивающие препараты, такие как ибупрофен, диклофенак и т. д. Люди часто изобретают новые версии этих лекарств в надежде, что у них будет меньше побочных эффектов или они будут обладать более сильным действием (или что их можно будет запатентовать и заработать деньги). В каждом испытании лекарство, произведенное спонсором, оказывалось лучше или по крайней мере не хуже, чем остальные, участвовавшие в исследовании. Ни в одном случае оно не оказалось хуже остальных. Философы и математики говорят о «переходности»: если А лучше В, а В лучше С, то С не может быть лучше, чем А. Но обзор 56 испытаний показал полный абсурд: все эти лекарства были лучше друг друга.
Но за углом нас ждет еще один сюрприз. Как ни удивительно, когда исследовались методологические недостатки, оказалось, что испытания, которые финансировались фармацевтической индустрией, использовали лучшие исследовательские методы, чем независимые испытания. Самое большее, что можно было предъявить фармкомпаниям, это такие мелочи, как использование неадекватных доз лекарств-конкурентов (как говорилось выше) или заявления в разделе «Выводы», которые преувеличивали положительность результатов. Но это были легко обнаруживаемые недостатки: нужно было только прочитать отчет об испытании, чтобы увидеть, что исследователи давали маленькую дозу обезболивающего; всегда следует читать разделы «Методы» и «Результаты», чтобы судить о данных исследования, поскольку разделы «Обсуждение» и «Выводы» в конце похожи на комментарии в газетах. Из них вы не узнаете ничего нового.
Как же мы можем объяснить тот факт, что результаты испытаний, финансируемых фармкомпаниями, часто такие блестящие? Каким образом все их лекарства одновременно оказываются лучшими? Самое главное может произойти после окончания испытаний.
Тенденциозность публикаций и подавление отрицательных результатов
Тенденциозность публикаций — это очень интересный и очень человеческий феномен. По ряду причин положительные результаты с большей вероятностью будут опубликованы, чем отрицательные. Это легко понять, если вы поставите себя на место исследователей. Во-первых, если результат отрицательный, вы чувствуете, что зря потеряли время. Легко убедить себя в том, что вы ничего не нашли, хотя в действительности вы нашли очень полезную информацию: вы узнали, что вещь, которую вы тестируете, не работает.
Правильно это или нет, но получение данных о том, что что- то не работает, конечно, не принесет вам Нобелевской премии — нет на свете справедливости, — поэтому у вас могут пропасть мотивация работать над этим проектом и появиться новые приоритеты. Вы не захотите публиковать свои отрицательные результаты в академическом журнале, и ваши данные будут пылиться на дне ящика письменного стола. Пройдут месяцы. Вы получите новый грант. Чувство вины вас будет иногда беспокоить, но понедельник — ваш день в клинике, значит, неделя начинается во вторник, а в среду встреча в департаменте, поэтому четверг — это единственный день, когда вы можете поработать, а в пятницу вы читаете лекции, и так пройдет год, ваш шеф уйдет на пенсию, а новый даже не будет знать о том, что проводился эксперимент, и так отрицательные результаты будут забыты навсегда. Если вы улыбаетесь, читая этот абзац, потому что узнали себя, то вы очень плохой человек.
Даже если вы опубликуете свои отрицательные результаты, это не будет новостью. Вы, вероятно, не сможете опубликовать их в самом известном журнале, если только это не крупные испытания чего-то, что обещало сенсацию, пока ваш отрицательный эксперимент все не испортил. Это уважительная причина, чтобы вы особенно не суетились, и это также означает, что весь процесс отложится на неопределенное время: ленивым журналам может потребоваться год, чтобы отвергнуть вашу статью. Каждый раз, когда вы будете подавать статью в разные журналы, вам придется переформатировать ссылки (часы утомительного труда). Если вы замахиваетесь высоко и получаете несколько отказов, могут пройти годы, пока статья выйдет, даже если вы очень старались, и все эти годы люди не будут знать о ваших исследованиях.
Тенденциозность публикаций весьма распространена и в некоторых областях встречается чаще, чем в других. В 1995 году только 1 % всех статей, опубликованных в журналах альтернативной медицины, содержал отрицательные результаты. Самая последняя цифра — это 5 % отрицательных публикаций. Это очень низкий процент, хотя, если быть честным, могло быть и хуже. Обзор 1998 года охватил весь спектр исследований китайской медицины и не нашел ни одной публикации, описывающей отрицательные результаты. Ни одной. Вы видите, почему я использую нетрадиционную и альтернативную медицину (НиАМ) как учебное пособие для изучения доказательной медицины.
В целом тенденциозность публикаций не проявляется так откровенно, и вы можете получить представление о том, что она существует в данной области, сделав очень умную вещь под названием funnel plot (диаграмма в виде воронки). Это потребует на короткое время вашего внимания.
Если есть множество исследований на одну тему, они должны дать слегка отличные друг от друга результаты, но можно ожидать, что все они будут близки к правильному. Вы также можете ожидать, что результаты более крупных испытаний с большим количеством участников и лучшими методами будут сосредоточены вокруг правильного ответа и ближе к нему, чем результаты мелких испытаний, а они, в свою очередь, будут разбросаны дальше, положительные и отрицательные, поскольку для исследования, скажем, с двадцатью участниками достаточно трех фальшивых результатов, чтобы сделать неправильные выводы.
Диаграмма в виде воронки помогает представить это наглядно. Вы обозначаете эффект на оси X слева направо. Затем на оси Y (сверху вниз) вы показываете, насколько большим было исследование, или каким-нибудь другим способом измеряете его точность. Если в публикациях нет никакого уклона, вы увидите прелестную перевернутую воронку: крупные, точные испытания будут сосредоточены вокруг ее вершины, а затем, по мере движения вниз, мелкие и менее точные будут постепенно распространяться вправо и влево, по мере снижения их точности — как положительные, так и отрицательные.
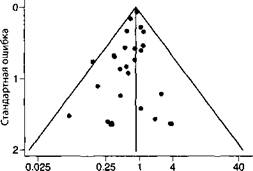
Уровень риска (смертность)
Однако если в публикациях есть тенденциозность, результаты будут асимметричными. Мелкие, некачественные отрицательные испытания будут отсутствовать, поскольку их будут игнорировать. Кажется, никто ничего не потеряет, если результаты этих крошечных, неубедительных испытаний так и останутся на дне ящика письменного стола, — таким образом, опубликованными оказываются только положительные результаты. Эта тенденциозность не только была продемонстрирована во многих областях медицины: одна статья обнаружила доказательства тенденциозности в самих исследованиях тенденциозности в публикациях. Вот воронкообразная диаграмма этой статьи. Такова ирония доказательной медицины.

Самый неприятный недавний случай этого явления — это исследования антидепрессантов СИОЗС, как было показано в различных статьях. Группа ученых в начале 2008 года опубликовала статью в «Медицинском журнале Новой Англии» (New England Journal of Medicine), где были перечислены все испытания СИОЗС, которые были официально зарегистрированы Управлением по контролю за качеством пищевых продуктов и лекарственных средств, и изучила эти испытания в научной литературе. Тридцать семь испытаний были оценены управлением как положительные: за исключением одного, все они были правильно описаны и опубликованы. Двадцать два испытания, которые показали отрицательные или неопределенные результаты, просто не были опубликованы, а одиннадцать были описаны и опубликованы таким образом, что их результаты выглядели положительными.
Это более чем нахально. Врачам нужна достоверная информация, если мы хотим, чтобы они принимали правильные и безопасные решения, когда прописывают лекарства. Утаивание от них этой информации и обман — это моральное преступление. Если бы я не писал сейчас несерьезную и забавную книгу о науке, я бы пришел в ярость.
Повторные публикации
Фармацевтические компании могут сделать лучше, чем проигнорировать отрицательные результаты. Иногда, когда испытания дают положительные результаты, они публикуют их несколько раз, в разных местах, в разных формах, так что они выглядят как разные. Это особенно легко, когда вы проводите крупное мультицентровое исследование, поскольку вы можете публиковать фрагменты испытаний по каждому центру отдельно или в разных перестановках. Это также очень удобный способ заставить данные работать на вас, поскольку читатель вряд ли сможет это проверить.
Классическое детективное расследование в этой области было проведено бдительным анестезиологом из Оксфорда Мартином Трамером (Martin Tramer), который изучал эффективность лекарства от тошноты, ондансетрона. Он заметил, что многие данные в метаанализе, который он делал, повторялись: результаты отдельных пациентов попадались ему несколько раз, в слегка отличной форме, в очевидно разных исследованиях и в разных журналах. Данные, которые показывали лекарство в наиболее выгодном свете, имели большую вероятность повторяться, чем те, которые выглядели менее убедительно, и это в конечном счете привело к переоценке эффективности лекарства на 23 %.
Сокрытие вреда
Вот так фармацевтические компании приукрашивают свои положительные результаты. А как насчет более темной стороны всего этого? Где они прячут серьезный вред?
Побочные эффекты — это жизненный факт: их следует воспринимать в контексте приносимой лекарством пользы и тщательно контролировать, поскольку непреднамеренные последствия лекарственных вмешательств могут быть очень серьезными. Громкие истории, которые привлекают всеобщее внимание, — это истории грязной игры или сокрытия фактов. Однако важные данные могут быть упущены и по более невинным причинам: вполне естественно проигнорировать тенденциозность в публикациях или не заметить беспокоящих фактов на фоне общего шума.
Лекарства против сердечной аритмии дают нам интересный пример. Люди, у которых бывают сердечные приступы, часто страдают аритмией (поскольку у них не в порядке естественный водитель сердечного ритма), и это может послужить причиной смерти. Антиаритмические препараты используются для лечения и предотвращения сбоев сердечного ритма у таких людей. Доктора подумали, что было бы неплохо давать их всем, кто перенес сердечный приступ. Это казалось разумным на бумаге, препараты выглядели безопасными, и в то время никто не знал, что на самом деле они увеличивают риск смерти в этой группе, поскольку с теоретической точки зрения это казалось нелогичным (как в случае с антиоксидантами). Но это оказалось правдой, и в середине 1980-х, на пике их использования, антиаритмические препараты вызывали количество смертей, сравнимых с общим количеством американцев, погибших во время вьетнамской войны. Информация, которая могла бы предотвратить эту трагедию, к сожалению, лежала на дне ящика письменного стола, как позже объяснил один из исследователей: «Когда мы провели наше исследование в 1980 году, мы думали, что повышенный уровень смертности был… результатом стечения обстоятельств. Разработка лекарства была прекращена по коммерческим причинам, и результаты этого исследования так и не были опубликованы. Сейчас это выглядит ярким примером тенденциозности. Результаты, описанные здесь, могли бы заранее предупредить об опасности».
Это была небрежность и предвзятое мышление. Но иногда кажется, что опасные эффекты лекарств могут быть намеренно преуменьшены или, что еще хуже, просто не опубликованы. Недавно погремел ряд скандалов, связанных с фармацевтической индустрией, по поводу того, что данные о вреде лекарств, включая Vioxx и антидепрессанты, намеренно не были оглашены. Правда вскоре вышла наружу, и тот, кто говорит, что медики не захотели выносить сор из избы, просто не в курсе ситуации. Эти данные, не забывайте, были в трех самых читаемых статьях в «Британском медицинском журнале». Стоит посмотреть на них еще раз попристальнее.
Vioxx
Vioxx — это обезболивающий препарат компании Merck, одобренный американским Управлением по контролю за качеством пищевых продуктов и лекарственных препаратов (FDA) в 1999 году. Многие обезболивающие вызывают проблемы с пищеварительным трактом — язвы и другие, — и производители надеялись, что новое лекарство не будет иметь таких побочных эффектов. Это было проверено в испытаниях, которые назывались VIGOR и сравнивали Vioxx с более старым препаратом напроксеном. В результате ожидалась большая прибыль. Испытание дало смешанные результаты. Vioxx не лучше снимал симптомы при ревматоидном артрите, но вдвое уменьшал риск желудочно- кишечных проблем, что было прекрасной новостью. Однако также был обнаружен повышенный риск сердечных приступов.
Однако когда результаты VIGOR были опубликованы, кардиологический риск куда-то исчез. Там был промежуточный анализ сердечных приступов и язвы, где язвы считались дольше, чем сердечные приступы. Это не было описано в публикации, и в результате преимущество Vioxx в отношении язв было преувеличено, а риск сердечных приступов преуменьшен. «Эта неприемлемая деталь плана клинических испытаний, которая, несомненно, исказила результаты, не стала известной издателям и научным авторам исследования», — отмечалось в большой и необычно критической редакционной статье в «Медицинском журнале Новой Англии» (New England Journal of Medicine). Было ли это проблемой? Безусловно. Например, еще три инфаркта миокарда произошли в группе Vioxx в течение месяца после того, как перестали фиксироваться сердечные побочные эффекты, в то время как в группе, принимавшей напроксен, за этот период произошел только один инфаркт.
Внутренний меморандум от Эдварда Скольника (Edward Scolnick), главного исследователя компании, показывает, что производителю было известно о кардиологическом риске («Это позор, но частота была низкая, и риск оказался зависимым от механизма лекарства, как мы и опасались»), «Медицинский журнал Новой Англии» не был этим удовлетворен и напечатал пару демонстративно критических статей.
Тревожное увеличение риска сердечных приступов на самом деле было обнаружено людьми, которые исследовали данные FDA; это то, чего врачи стараются не делать — во всяком случае, когда читают научные статьи. В попытке объяснить умеренное повышение риска сердечных приступов, которое можно было обнаружить в итоговой статье, авторы предложили «напроксеновую гипотезу»: Vioxx не вызывал сердечных приступов, зато напроксен их предотвращал. Тем не менее нет никаких доказательств, что напроксен обладает профилактическим действием против сердечных приступов.
Во внутреннем меморандуме, который обсуждался достаточно подробно в статьях, посвященных этому случаю, говорилось, что компания была обеспокоена. В конце концов, появилось больше доказательств вреда Vioxx, и препарат был отозван с рынка в 2004 году. Однако анализ FDA показал, что за пять лет продаж это лекарство вызвало от 88 000 до 139 000 сердечных приступов, от 30 до 40 % которых, возможно, были фатальными.
Трудно сказать, можно ли доверять этой цифре, но судя по тому, как информация вышла наружу, чувствуется, что и сама компания Merck, и FDA могли бы сделать гораздо больше, чтобы уменьшить вред, нанесенный за годы использования лекарства, после того как им стали очевидны возможные риски. Трудно переоценить значение данных в медицине: они означают жизни людей. Фирма «Мерк» не признала ответственности и предложила урегулировать вопрос в США за 4,85 миллиарда долларов.
Авторы, которым запрещают публиковать данные
Все это звучит достаточно мрачно. Какие исследователи этим занимаются и почему мы не можем их остановить? Некоторые из них, конечно, обманщики. Но на многих оказывают давление, запрещая им раскрывать информацию об испытаниях, которые они проводят на средства фармацевтических компаний.
Вот два экстремальных примера того, что, как это ни трагично, является достаточно распространенным явлением. В 2000 году американская компания выдвинула обвинение против ведущих исследователей и их университетов в попытке заблокировать публикацию исследования вакцины против ВИЧ, в котором обнаружилось, что эта вакцина действует не лучше, чем плацебо. Исследователи считали, что они должны проинформировать об этом пациентов. Компания считала иначе. Результаты были опубликованы в «Журнале Американской медицинской ассоциации» в том же году.
Второй пример. Нэнси Оливьери (Nancy Olivieri), директор программ по гемоглобинопатиям в Торонто, проводила клинические испытания деферипрона, препарата, удаляющего излишек железа из организма пациентов, у которых возник его избыток в результате многочисленных переливаний крови. Она забеспокоилась, когда увидела, что концентрация железа в печени у некоторых пациентов недостаточно контролировалась и был превышен порог безопасности для сердечно-сосудистых заболеваний и преждевременной смерти. Более обширные исследования заставили предположить, что деферипрон может ускорить развитие фиброзных изменений в печени.
Фармацевтическая компания Apotex неоднократно письменно угрожала Оливьери, что, если она опубликует эти данные и свои опасения, они подадут на нее в суд. С большим мужеством — и, к стыду университета, без его поддержки — Оливьери представила свои результаты на нескольких научных конференциях и в академических журналах. Она считала себя обязанной поделиться своими данными и опасениями, невзирая на личные последствия. Необходимо сделать все, чтобы ученым не приходилось в одиночку принимать такие решения.
Одно-единственное недорогое решение всех проблем во всем мире
Поистине необыкновенно, что почти все эти проблемы — замалчивание отрицательных результатов, манипуляции с данными и тому подобное — могли бы быть решены с помощью одного очень простого акта, который не будет стоить практически ничего: введения реестра клинических испытаний, публичного, открытого и обязательного для всех. Вот как он будет работать. Вы — фармацевтическая компания. Прежде чем вы начнете ваше исследование, вы публикуете его протокол в каком-нибудь публичном издании. Это означает, что любой может увидеть, что вы собираетесь делать в ваших исследованиях, что именно вы собираетесь определить, сколько будет участников и т. д. еще до начала испытаний.
Проблемы тенденциозности в публикациях, повторные публикации, скрытые данные о побочных эффектах, которые приводят к необязательным смертям и страданиям, — все это будет искоренено одним махом. Если вы зарегистрировали испытание и провели его, но оно не появилось в литературе, это сразу будет очевидно. Естественно, что все подумают, что вам есть что скрывать (возможно, они будут правы). Сейчас тоже есть реестры испытаний, но они в полном беспорядке.
Насколько там отсутствует порядок, видно из примера с последней уловкой фармацевтических компаний: сменой целей.
В 2002 году компании Merck и Schering Plough начали испытания эзетимиба, лекарства, предназначенного для снижения холестерина. Сначала они заявили, что собирались измерять один параметр: работает ли лекарство, но затем, когда были получены результаты, они сказали, что на самом деле измеряли совершенно другие вещи. Это было замечено, и они получили публичный выговор. Почему? Потому что если вы измеряете много параметров (как они и делали), некоторые могут оказаться положительными просто случайно. Вы не можете найти вашу стартовую гипотезу в конечных результатах. Это делает всю статистику ненадежной.
Реклама
«Таблетки кломикалма являются единственным лекарством, одобренным для лечения беспокойства у собак».
В Великобритании нет рекламы лекарств, адресованной непосредственно покупателю, и это позор, поскольку американская реклама чрезвычайно любопытна, особенно телевизионные ролики. У вас все валится из рук, ваши беспокойные ноги/ мигрень/холестерин вас замучили, вы страдаете, жизнь потеряла смысл. Затем вы принимаете правильную таблетку, и экран вдруг становится ярким, теплого желтого цвета, бабушка смеется, дети смеются, собака машет хвостом, ребенок, который мучился животом, играет на лужайке со шлангом, водяные струи сияют радугой на солнце, а он смеется, и все родственники счастливы. Жизнь прекрасна.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Уже и официальная медицина обращается к народной
Уже и официальная медицина обращается к народной Столько сейчас говорят про народные методы лечения, что уже и официальная медицина к ним обращаться начинает. Очищение кишечника и печени плюс уринотерапию мне порекомендовал мой участковый врач. Я в чудеса не верил. Но
Медицина, которой пользуются люди, потребляющие вареную пищу, является всецело ошибочной наукой
Медицина, которой пользуются люди, потребляющие вареную пищу, является всецело ошибочной наукой Как мы видим, болезни возникают в организме в результате нехватки или полного отсутствия сырых материалов. Здоровье может быть сохранено лишь в том случае, когда сырые
Официальная медицина – главное препятствие на пути утверждения новой парадигмы безлекарственного здравоохранения
Официальная медицина – главное препятствие на пути утверждения новой парадигмы безлекарственного здравоохранения О значении лекарств в жизни человекаЗнаменитый древнегреческий врач Гиппократ говорил так: «Болезнь лечит врач, но излечивает Природа».Итак, болезнь
Официальная медицина против новых идей
Официальная медицина против новых идей В условиях, когда лекарства себя изживают, на смену традиционной медицине идет медицина естественная. На смену старой парадигме лекарственного здравоохранения идет новая парадигма безлекарственного лечения болезней.Новая
СОН: ЧЕМ ОН ЯВЛЯЕТСЯ И ЧЕМ НЕ ЯВЛЯЕТСЯ
СОН: ЧЕМ ОН ЯВЛЯЕТСЯ И ЧЕМ НЕ ЯВЛЯЕТСЯ Во время сна тело находится в состоянии глубокого покоя, метаболизм снижается, а мозг перестает осознавать окружающий нас мир.Спящий мозг отнюдь не становится полностью бессознательным, он просто смещает направление сознания,
5.3. А что говорит официальная медицина?
5.3. А что говорит официальная медицина? Впервые я прошла диагностическое обследование спустя год после отказа от приёма пищи и жидкости на кафедре медицинского факультета Университета Дружбы народов у доктора медицинских наук, профессора А. Я. Чижова. Исследование
Является ли токсичность проблемой для вас?
Является ли токсичность проблемой для вас? Существует множество симптомов, являющихся результатом влияния токсинов. Однако вам нужно сосредоточивать внимание только на тех из них, которые являются хроническими. Они могут включать в себя постоянное чихание, насморк,
Что является лекарственным сырьем?
Что является лекарственным сырьем? Лекарственным сырьем могут служить все части этого замечательного растения. Помимо плодов, в лечении различных болезней используются цветы, побеги, корни, семена
Что говорит официальная медицина
Что говорит официальная медицина Несмотря на огромное количество проверенных многими народами и временем целебных свойств топинамбура, официальной медициной в достаточном большом объеме было исследовано лишь одно его применение – лечение людей, страдающих сахарным
Официальная медицина — главное препятствие на пути утверждения новой парадигмы безлекарственного здравоохранения
Официальная медицина — главное препятствие на пути утверждения новой парадигмы безлекарственного здравоохранения О значении лекарств в жизни человекаЗнаменитый древнегреческий врач Гиппократ говорил так: «Болезнь лечит врач, но излечивает Природа».Итак, болезнь
Холистическая медицина — энергетическая медицина будущего
Холистическая медицина — энергетическая медицина будущего Холистическая медицина как комплекс медицинских систем — это сочетание разных взглядов на то, как надо лечить человека, с их разными подходами, разными понятийными аппаратами, разной терминологией, разной
Для тех, кому не может помочь официальная медицина. Дыхательная гимнастика А. Н. Стрельниковой
Для тех, кому не может помочь официальная медицина. Дыхательная гимнастика А. Н. Стрельниковой Александра Николаевна Стрельникова – оперная певица и талантливый театральный педагог. В молодости она потеряла голос. Ее мать помогла его вернуть с помощью специально
Какой вес является нормальным
Какой вес является нормальным Сейчас это очень актуальный вопрос. Равнение на моделей привело к тому, что девушки считают излишним любой вес, если при нем не выпирают кости, а женщины старшего возраста говорят «не от котлет, а от лет» и живут с излишним весом, который