Фибринолитическая (плазминовая) система
Фибринолитическая (плазминовая) система
Ферментная система, обеспечивающая растворение фибрина в кровяном русле, получила название фибринолитической, или плазминовой, системы. Это растворение осуществляется основным компонентом указанной системы – фибринолизином (или плазмином), который в плазме содержится в виде профермента (плазминогена) в концентрации около 20,6 + 3,6 мг%. Как в плазме, так и в тканях плазминоген содержится в виде двух или более молекулярных форм, отличающихся друг от друга способами выделения, особенностями активации и инактивации. Каждая из двух основных форм состоит из нескольких молекулярных подформ:
1) нативный плазминоген с NH2-терминальной глютаминовой кислотой – «глю-плазминоген»;
2) подвергшийся ограниченному протеолизу плазминоген с NH2-терминальным лизином, валином или метионином – «лиз-плазминоген». Лиз-плазминоген в 10–20 раз быстрее трансформируется активаторами в плазмин, имеет значительно более выраженное, чем глю-плазминоген, сродство к фибрину и значительно быстрее последнего метаболизируется – его Т1/2 в циркуляции около 0,8 суток, а глю-плазминогена – 1,24 ± 0,29 суток. По механизму протеолитического действия плазмин наиболее близок к трипсину.
После активации плазминоген быстро исчезает из кровотока – блокируется антиплазминами и удаляется. Вслед за введением больших доз стрептокиназы или урокиназы уровень плазминогена в крови снижается до нуля, но затем в течение 12–28 ч восстанавливается, если прекращена его дальнейшая активация.
Эта способность активаторов фибринолиза быстро истощать запасы плазминогена в крови и на время оставлять больного без ферментативного фибринолиза важна для клиники и должна учитываться при лечении тромбозов и синдрома диссеминированного внутрисосудистого свертывания крови.
Существующие в организме механизмы активации плазминогена весьма разнообразны, но, подобно механизмам свертывания крови, они также могут быть подразделены на две основные группы – с внутренней и внешней активацией.
Ведущий внутренний механизм запускается теми же факторами, какие инициируют свертывание крови, а именно фактором ХIIа, который, взаимодействуя с прекалликреином и высокомолекулярным кининогеном плазмы (ВМК), активирует плазминоген. Такой путь фибринолиза – базисный, обеспечивающий активацию плазминовой системы не вслед за свертыванием крови, а одновременно с ним. Он функционирует по «замкнутому циклу», поскольку образующиеся первые порции калликреина и плазмина вызывают протеолиз фактора XII, отцепляя фрагменты, под действием которых нарастает изменение прекалликреина в калликреин. Такая интенсивная самоактивация приводит к тому, что ХIIа-калликреин-зависимый фибринолиз при интенсивном внутрисосудистом свертывании крови истощается быстро, раньше других механизмов фибринолиза.
Лимитирующими факторами являются в первую очередь ВМК и прекалликреин. Их плазменный резерв быстро истощается, тогда как уровень плазминогена остается в крови еще достаточно высоким. В таких условиях ХIIа-зависимый фибринолиз уже не функционирует, но поддается другим (не калликреиновым) способам активации – стрептокиназой и урокиназой. Лишь вслед за этим возможно истощение запасов плазминогена, что делает неэффективным любые способы активации плазминовой системы. Определенное участие в активации внутреннего механизма фибринолиза принимает, по-видимому, и фактор Виллебранда. В частности, на образцах плазмы с дефицитом ВМК показано, что фактор Виллебранда в 2–3 раза усиливает превращение прекалликреина в калликреин под влиянием фрагментов фактора XII. В присутствии ВМК, обладающего значительно более мощным влиянием на активацию прекалликреина, это действие фактора Виллебранда становится малоощутимым.
Заслуживает внимания то обстоятельство, что если в свертывании крови компонентам калликреин-кининовой системы отводится в определенной мере вспомогательная функция, то в гуморальном механизме фибринолиза это один из ведущих механизмов. Возможно, именно поэтому при генетически обусловленном дефиците плазменного прекалликреина (дефект Флетчера) или ВМК (дефект Фитцжеральда – Вильсона) у больных нет кровоточивости и вместе с тем прослеживается наклонность к тромбозам.
Важнейшими стимуляторами внешнего механизма фибринолиза являются белковые активаторы плазминогена, синтезируемые в сосудистой стенке. Эти активаторы подразделяются на высокомолекулярные и низкомолекулярные фракции, обнаруживают высокое сродство к фибрину. Физиологическая регуляция синтеза и выделения в кровь сосудистых активаторов изучена недостаточно. Тем не менее известно, что их интенсивный выброс происходит при нарушении проходимости сосудов, в том числе и при пережатии сосуда манжетой, а также при физических нагрузках, под влиянием вазоактивных веществ. Определение эуглобулинового лизиса до и после пережатия сосуда (манжеточная проба) используется для оценки резерва сосудистых активаторов плазминогена и функциональной полноценности механизмов их либерации. Депрессия данных механизмов характерна для ряда тромбофилических состояний. Стероидные гормоны анаболического действия повышают синтез в эндотелии активаторов фибринолиза, с чем отчасти связывается их благоприятное влияние на течение флеботромботической болезни.
Мощные активаторы плазминогена содержатся также в клетках крови – эритроцитах, тромбоцитах и особенно лейкоцитах. При внутрисосудистом свертывании крови, тромбообразовании, воздействии эндотоксином, активации системы комплемента, гемолизе эти активаторы освобождаются из клеток в «плазматическую атмосферу» и активируют плазминоген.
Более того, установлено, что гранулоциты секретируют не только активатор плазминогена, но и внутриклеточные протеазы (цитокиназы), которые самостоятельно, без участия плазмина, переваривают фибрин. При этом образуются иные продукты расщепления фибрина, чем при его плазминовом расщеплении.
Следовательно, лейкоциты обеспечивают функционирование самостоятельного (неплазминового) механизма растворения фибрина. Этот альтернативный механизм играет важную роль в ограничении размеров тромбов и в деблокировании микроциркуляторного русла при диссеминированном внутрисосудистом свертывании крови.
Разнообразные активаторы плазминогена (цитокиназы) содержатся и в других тканях и клетках, особенно в эпителиальной, мышечной и мезенхимальной, а также в секретах и экскретах – моче, молоке, желчи, слюне. Некоторые из них поступают в определенных количествах в кровь, участвуя в активации плазминогена. В частности, таким свойством обладает урокиназа – активатор фибринолиза, синтезируемый в почечном эпителии и выделяющийся с мочой. В кровь поступает небольшое количество урокиназы, ответственное приблизительно за 10–15% общей плазминоген-активаторной функции. В настоящее время установлено, что большинство тканевых активаторов плазминоген идентично сосудистому, эндотелиальному.
Фибринолиз ингибируется рядом антиактиваторов и антиплазминов, из которых наиболее важен недавно открытый быстродействующий антиплазмин, относящийся к ?2-глобулинам (молекулярная масса 65 000–70 000) и содержащийся в плазме в количестве 70 мг/л. Этого количества достаточно, чтобы нейтрализовать более 2/3 всего плазмина, образующегося при максимальной активации плазминогена. Однако плазмин, связанный с фибрином, хуже комплексируется с антиплазмином, чем при циркуляции в свободном состоянии. Антиплазмин ослабляет процесс связывания плазминогена с фибрином. Присутствие в плазме циркулирующих комплексов плазмин – антиплазмин, как и комплексов тромбин-ATIII, служит признаком интенсивного внутрисосудистого свертывания крови и активации фибринолиза. Выявление этих комплексов облегчается тем, что в них появляются новые антигенные свойства (так называемые неоантигены).
Быстродействующий ?2-антиплазмин обладает также антиактиваторным действием, но он не идентичен другому антиактиватору, описанному Hedner (1973, 1977 гг.).
Из других ингибиторов фибринолиза, обладающих значительно более слабым действием, заслуживают упоминания ?2-макроглобулин и ингибитор С1-эстеразы. Последний ингибирует фактор ХIIа, калликреин и отчасти плазмин, специфически блокирует внутренний (ХIIа-зависимый) фибринолиз. Вместе с тем имеются данные о том, что ?2-макроглобулин не столько препятствует фибринолизу, сколько защищает плазмин от других, более мощных, ингибиторов. В частности, комплекс макроглобулин-плазмин защищен от быстродействующего ?2-антиплазмина, благодаря чему при активации плазминовой системы идет лизис не только фибрина и РФМК, но в небольшой степени и фибриногена, хотя в плазме имеется избыток ?2-антиплазмина.
Плазминовая система специфически адаптирована к лизису фибрина и растворимых фибрин-мономерных комплексов (РФМК), хотя при ее значительной активации расщеплению подвергаются и другие белки (в том числе факторы свертывания V и VIII).
Механизм преимущественной активации фибринолиза в тромбах и сгустках, резко выраженного преобладания фибринолиза над фибриногенолизом пока не может считаться окончательно выясненным. Твердо доказана лишь способность частично активированного плазминогена (лиз-плазминогена) связываться с фибрином. Установлено также, что растворение идет тем быстрее, чем выше локальная концентрация в сгустках плазминогена. Особенно важно, что сосудистый активатор плазминогена также концентрируется на фибрине. Наконец, установлено, что ?2-антиплазмин намного слабее инактивирует связанный с фибрином плазмин, тогда как циркулирующий «свободный» плазмин образует с этим мощным ингибитором плохо диссоциирующие комплексы.
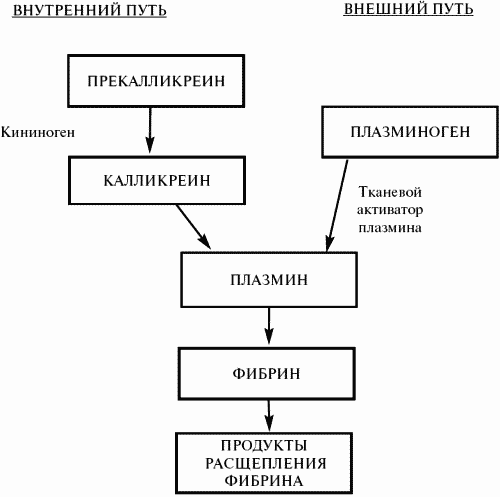
Схема 3 Фибринолитическая система
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКДанный текст является ознакомительным фрагментом.
Читайте также
14. ВЕНЫ ВЕРХНЕЙ КОНЕЧНОСТИ. СИСТЕМА НИЖНЕЙ ПОЛОЙ ВЕНЫ. СИСТЕМА ВОРОТНОЙ ВЕНЫ
14. ВЕНЫ ВЕРХНЕЙ КОНЕЧНОСТИ. СИСТЕМА НИЖНЕЙ ПОЛОЙ ВЕНЫ. СИСТЕМА ВОРОТНОЙ ВЕНЫ Эти вены представлены глубокими и поверхностными венами.В поверхностную ладонную венозную дугу (arcus venosus palmaris superficialis) впадают ладонные пальцевые вены.В глубокую ладонную венозную дугу (arcus venosus
Нервная система как система власти
Нервная система как система власти Проблема власти и организации является основной проблемой в деятельности нервной системы. Задачи этой системы сводятся к организации и управлению процессами, происходящими внутри организма и между организмом и его средой. Тот факт,
3.1. Пирамидная система
3.1. Пирамидная система Различают два основных вида движений: непроизвольные и произвольные.К непроизвольным относятся простые автоматические движения, осуществляемые за счет сегментарного аппарата спинного мозга и мозгового ствола по типу простого рефлекторного акта.
3.2. Экстрапирамидная система
3.2. Экстрапирамидная система Термином «экстрапирамидная система» обозначают подкорковые и стволовые внепирамидные образования и моторные пути, которые не проходят через пирамиды продолговатого мозга. Частью этой системы также являются те пучки, которые связывают кору
3.3. Мозжечковая система
3.3. Мозжечковая система Мозжечок и ствол мозга занимают заднюю черепную ямку, крышей которой является намет мозжечка. Мозжечок соединяется со стволом мозга тремя парами ножек: верхние мозжечковые ножки соединяют мозжечок со средним мозгом, средние ножки переходят в
Система Пилатеса
Система Пилатеса Многим спортсменам, артистам балета и даже звездам помогла гимнастика по системе Джозефа Пилатеса.Ее автор родился недалеко от Дюссельдорфа в Германии. Как это часто бывает, люди, добивающиеся чего-то в жизни, в детском возрасте бывают слабыми и
Индийская система
Индийская система Знаменитый индийский доктор Феридун Батмангхелидж и его ученик Ранжит Моханти уверены, что большинство болезней, в том числе и болезни спины, происходят от… жажды.Д-р Феридун Батмангхелидж родился в 1931 году в Иране. Он прекрасно учился и успешно
4.3. Противосвертывающая система
4.3. Противосвертывающая система За сохранение крови в жидком состоянии отвечают естественные вещества, которые обладают противосвертывающими свойствами. Эти вещества постоянно вырабатываются в организме и в необходимом количестве с определенной скоростью выделяются
4.4. Фибринолитическая система
4.4. Фибринолитическая система Функция фибринолитической системы заключается в разрушении фибрина. В роли же главного компонента фибринолитической системы выступает плазмин (фибринолизин), который образуется из плазминогена под действием различных активаторов
Эндокринная система
Эндокринная система Эндо – внутри, кринис – секрет (греч.). Основной функцией эндокринной системы является воспроизводство и хранение гормонов в органах, называемых железами внутренней секреции. Эти железы: надпочечники, гипоталамус, поджелудочная железа, яичники,
Глава IV. Двойная система соответствия голове. Система "насекомого". Минисистема
Глава IV. Двойная система соответствия голове. Система "насекомого". Минисистема Двойная система соответствия головеНа пальцах кистей и стоп располагаются две системы соответствия голове: система "типа человека" и система "типа животного".Система "типа человека".Граница
Система чакр
Система чакр Верхний энергетический центр, седьмая чакра, сахасрара Эта чакра, верхний энергетический центр, имеет вход в области макушки, там, где находится родничок. Через сахасрару мы воспринимаем потоки Божественной энергии, поддержку свыше, защиту от
Первый эмоциональный центр — костная система, суставы, кровообращение, иммунная система, кожа
Первый эмоциональный центр — костная система, суставы, кровообращение, иммунная система, кожа Здоровое состояние органов, связанных с первым эмоциональным центром, зависит от ощущения безопасности в этом мире. Если вы лишены поддержки семьи и друзей, которая вам
Оздоровительная система дао
Оздоровительная система дао Древнекитайская система дао направлена на общее оздоровление организма и сохранение молодости. Упражнения по укреплению зрения и лечение различных заболеваний глаз, входящие в эту систему, рекомендуется выполнять при любых аномалиях
Система Ниши – еще одна система восстановления капилляров
Система Ниши – еще одна система восстановления капилляров Залманов – не единственный человек, который пришел к мысли о важности капилляров. Японский инженер Кацудзо Ниши, последовав вслед за Залмановым, создал свою методику здоровья, основанную на работе с